-
下列实验基本操作或事故处理,正确的是( )
A. 实验用剩的试剂都不能放回原试剂瓶,以防污染试剂
B. 眼睛里溅入酸溶液立即用水冲洗再涂抹1%-3%的NaHCO3溶液
C. 在气体发生装置上直接点燃氢气时,必须先检验氢气的纯度
D. 配制硫酸溶液时先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
难度: 简单查看答案及解析
-
下列检验或实验操作正确的是( )
A. 加入AgNO3溶液有白色沉淀生成,证明原溶液中一定有Cl-
B. 加入稀HNO3酸化的BaCl2溶液,有白色沉淀生成,证明原溶液中一定有SO42-
C. 向某溶液中加入Ba(NO3)2溶液无明显现象,再滴入几滴硝酸酸化的AgNO3溶液,产生白色沉淀,证明原溶液中含有Cl-
D. 加入CaCl2溶液有白色沉淀生成,证明原溶液中一定有CO32-
难度: 中等查看答案及解析
-
下列实验中,所采取的分离方法与对应原理都正确的是( )
选项
目的
分离方法
原理
A
分离植物油和水
萃取
植物油和水互不相溶
B
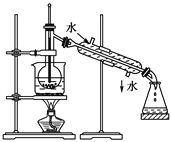
除去丁醇(沸点为117.5 ℃)中的乙醚(沸点为34.6 ℃)
蒸馏
丁醇与乙醚的沸点相差较大
C
分离水和乙醇
分液
水和乙醇的密度不同
D
分离溶于水中的碘
乙醇萃取
碘在乙醇中的溶解度较大
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列叙述正确的是( )
A. 物质的量是一个物理量,它的数目为NA
B. H2SO4的摩尔质量等于98
C. 利用气体摩尔体积计算时,气体可以是纯净物也可以是混合物
D. 将40gNaOH固体溶于1L水中配成溶液,溶液中氢氧化钠的浓度为1mol/L
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是
A. 在标准状况下,NA个CCl4分子所占体积为22.4L
B. 标准状况下任意比例混合的CH4与CO2的混合物22.4L,所含有的分子数为NA
C. 0.5mol/L的MgCl2溶液中含有的Cl—数为NA
D. 常温常压下,28g氮气含有的核外电子数为10NA
难度: 中等查看答案及解析
-
将标准状况下的a L HCl(气)溶于1000g水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度是( )
A.
mol/L B.
mol/L
C.
mol/L D.
mol/L
难度: 中等查看答案及解析