-
下列物质属于氧化物的是( )
A. 氧气 B. 水 C. 硫酸 D. 氯化钾
难度: 中等查看答案及解析
-
下列有关金属及其合金的说法正确的是( )
A. 硬铝的硬度比铝的硬度小
B. 不锈钢的抗腐蚀性能比纯铁好
C. 部分浸入水中的铁钉不易生锈
D. 防止金属腐蚀是保护金属资源的唯一途径
难度: 简单查看答案及解析
-
下列不属于化石燃料的是( )
A. 煤 B. 天然气 C. 石油 D. 汽油
难度: 简单查看答案及解析
-
一辆严重超载货车在急速下坡时轮胎发生燃烧,导致货车起火,造成人员和财产的重大损失.造成货车起火的直接原因是( )
A. 货车轮胎与空气接触
B. 超载货车轮胎与道路摩擦温度升高达到着火点
C. 货车在下坡车速较快
D. 制造轮胎的橡胶是可燃物
难度: 中等查看答案及解析
-
欲配制溶质质量分数为10%的NaCl溶液,下列操作不会导致溶液中NaCl质量分数小于10%的是( )
A. 在溶解氯化钠固体时用玻璃棒搅拌加速溶解
B. 烧杯先用少量蒸馏水润洗后再配制溶液
C. 称量氯化钠时,游码不在零位置就调节天平平衡,后将游码移动得到读数
D. 试剂瓶用蒸馏水润洗后再盛装配好的溶液
难度: 中等查看答案及解析
-
下列客机上使用的物品中,属于合成材料的是( )
A. 合金门把手 B. 真皮椅套 C. 塑料快餐盒 D. 羊毛毯子
难度: 简单查看答案及解析
-
诗词是中华民族灿烂文化中的瑰宝.用化学的观点解释下列著名诗句,错误的是( )
A. 蜡炬成灰泪始干:只发生化学变化
B. 为有暗香来:分子在不断运动;
C. 粉身碎骨浑不怕:生石灰变成熟石灰
D. 春蚕到死丝方尽:丝的成分是蛋白质
难度: 简单查看答案及解析
-
化学科学的发展促进了人类社会进步,提高了人们的生活质量.下列与人类社会进步相关的重大问题,其中和化学密切相关的是
①环境保护 ②能源开发利用 ③功能材料研究 ④生命过程探索( )
A. ①② B. ②③④ C. ①②③ D. ①②③④
难度: 简单查看答案及解析
-
下列变化属于化学变化的是( )
A. 石蜡熔化 B. 潮湿的衣服被晒干了
C. 钢铁生锈 D. 水变成水蒸气
难度: 简单查看答案及解析
-
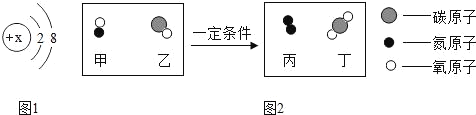
某物质在空气中燃烧的化学方程式为2X+3O2
2CO2+4H2O,下列说法正确的是( )
A. O2中氧元素的化合价为﹣2
B. 该反应属于置换反应
C. X属于有机物
D. CO2中碳、氧元素的质量比为1:2
难度: 中等查看答案及解析
-
实验操作正确的是( )
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
科学实验必须按规范进行操作,下列实验操作规范的是( )
A.
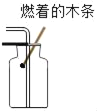 CO2验满 B.
CO2验满 B. 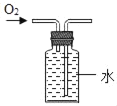 收集O2
收集O2C.
 滴加液体 D.
滴加液体 D.  测溶液pH
测溶液pH难度: 中等查看答案及解析
-
下列图标中,表示“禁止烟火”的是( )
A.
 B.
B. 
C.
 D.
D. 
难度: 简单查看答案及解析
-
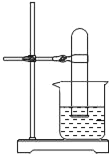
下列实验能达到目的是( )
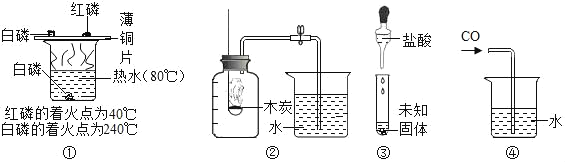
A. ①验证可燃物燃烧的条件
B. ②测定空气中O2的含量
C. ③检验CO32﹣的存在
D. ④用水吸收CO
难度: 中等查看答案及解析
-
以下部分化学实验的改进,不能达到实验目的是( )
A
B
C
D
改进后实验

燃烧条件

CO还原氧化铜

测定氧气含量

检验气密性
目的
防止燃烧产物污染空气
防止尾气对大气的污染
不用酒精灯点燃,使测定结果更精确
现象更明显
A. A B. B C. C D. D
难度: 困难查看答案及解析