-
在金属表面覆盖保护膜是普遍采用的金属防锈措施之一。下列自行车的防锈措施中,不属于覆盖保护膜的是
A.擦拭保持洁净与干燥 B.链条上油
C.轮圈镀铬 D.车架喷漆
难度: 简单查看答案及解析
-
在盛有水的烧杯中加入以下某种物质,形成溶液的过程中,温度下降。这种物质是
A.氢氧化钠 B.氯化钠 C.浓硫酸 D.硝酸铵
难度: 简单查看答案及解析
-
20℃时,氯化钠的溶解度为36g。对这句话理解错误的是
A.20℃时,100g水中最多能溶解氯化钠36g
B.20℃时,100g氯化钠饱和溶液中含氯化钠36g
C.20℃时,氯化钠饱和溶液中水与氯化钠的质量比为100:36
D.20℃时,将36g氯化钠溶解于100g水中,所得溶液为该温度下氯化钠的饱和溶液
难度: 简单查看答案及解析
-
生活中常见的下列物质,不属于溶液的是( )。
A. 糖水 B. 蒸馏水
C. 碘酒 D. 汽水
难度: 中等查看答案及解析
-
对于多数固体溶质的不饱和溶液,要使之成为饱和溶液,可采用的方法有( )
①降低温度;②升高温度;③加同种溶质;④加溶剂;⑤恒温蒸发溶剂.
A. ①③⑤ B. ②③④ C. ①②③ D. ②③⑤
难度: 中等查看答案及解析
-
实验室现有足量的20%的NaOH的溶液和蒸馏水,欲配制10%的NaOH溶液100g,需要20%的NaOH溶液( )
A. 95 g B. 50 g C. 100 g D. 10 g
难度: 简单查看答案及解析
-
按酸、碱、盐、氧化物的分类,下列各组物质属于一类的是( )
A. 氯化钠和碳酸钙 B. 氢氧化钠和硝酸钾
C. 氧化镁和氯化氢 D. 氧化钙和氢氧化钙
难度: 中等查看答案及解析
-
下列物质长时间敞口放置在空气中,质量增加并发生化学反应的是:( )
①烧碱 ②生石灰 ③浓盐酸 ④浓硫酸 ⑤熟石灰 ⑥铁钉.
A. ①②④ B. ①②⑤ C. ①②⑤⑥ D. ①②④⑤⑥
难度: 中等查看答案及解析
-
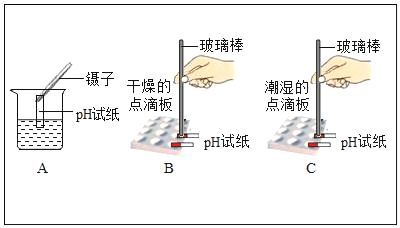
用pH试纸测定某溶液的酸碱度时,如果先用水把试纸润湿,再把溶液滴在试纸上,则测得的结果与实际的pH比较( )
A. 偏低 B. 偏高 C. 不变 D. 无法比较
难度: 简单查看答案及解析
-
混有水蒸汽的下列气体,既能用浓硫酸干燥,又能用固体氢氧化钠干燥的是( )
A. 二氧化碳 B. 氨气 C. 氧气 D. 氯化氢气体
难度: 简单查看答案及解析
-
若不用指示剂,要把氯化钙中少量的盐酸除去,使溶液达到中性,最好先用下列试剂( )
A. Ca(OH)2溶液 B. CaO
C. CaCO3 D. NaOH溶液
难度: 中等查看答案及解析
-
A、B、C三种不含结晶水的固体物质的溶解度曲线如图,下列说法中不正确的是

A. t1℃时,A的饱和溶液65 g中含有溶剂50 g ;
B. t2℃时, 将A、B、C三种物质的饱和溶液降温至t1℃,C溶液中溶质的 质量分数保持不变;
C. 在t2℃,A、B两种溶液中溶质的质量分数相同;
D. 要从B溶液中得到B通常可采用蒸发溶剂使其结晶的方法。
难度: 中等查看答案及解析
-
要增大CO2在水中的溶解度,可采用的方法是( )
A. 加压降温 B. 加压升温 C. 减压降温 D. 减压升温
难度: 简单查看答案及解析
-
A图是物质M和N的溶解度曲线.B图中甲、乙试管分别盛有M、N的饱和溶液,试管底均有未溶解的M、N固体.向烧杯中加入一种物质后,甲中的固体减少,乙中的固体增加,则加入的物质不可能是( )

A. 浓硫酸 B. 硝酸铵固体 C. 氧化钙 D. 氢氧化钠固体
难度: 中等查看答案及解析