-
要将一瓶接近饱和的石灰水变成饱和溶液,小明选择了如下方法,其中可行的是( )
①加入CaO ②加入Ca(OH)2 ③升高温度 ④降低温度
A. ②③ B. ②④ C. ①②③ D. ①②④
难度: 中等查看答案及解析
-
能验证 Zn、Cu、Ag 三种金属活动性顺序的一组试剂是
A. Zn、Ag、CuSO4溶液
B. Zn、Cu、Ag、H2SO4溶液
C. Cu、Ag、ZnSO4溶液
D. Ag、ZnSO4溶液、CuSO4溶液
难度: 中等查看答案及解析
-
下列有关物质的化学式、名称、俗名不完全对应的是( )
A. NaCl 氯化钠 食盐
B. CaO 氧化钙 熟石灰
C. C2H5OH 乙醇 酒精
D. NaOH 氢氧化钠 烧碱
难度: 简单查看答案及解析
-
下了有关实验现象或事实叙述错误的是( )
A.切完西瓜的菜刀洗净擦干放在通风干燥处可以防止生锈
B.铁丝在氧气中燃烧,火星四射,生成黑色固体
C.用黄铜片(铜锌合金)和铜片相互刻画,黄铜片上留有划痕
D.将二氧化碳通入燃着的两支高低蜡烛的烧杯中,蜡烛自低到高依次熄灭
难度: 中等查看答案及解析
-
要使右图装置中的小气球鼓起来,则使用的固体和液体可以是

①硝酸铵和水; ②铁和稀硫酸; ③固体氢氧化钠和水;
④生石灰和水; ⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.②③⑤ D.②④⑤
难度: 困难查看答案及解析
-
一定温度下,向图I烧杯中加入一定量的水,如图Ⅱ所示,所得溶液与原溶液相比,下列判断一定正确的是( )

A. 所得溶液是饱和溶液 B. 溶质的质量分数变大
C. 溶质的质量增加 D. 溶质的溶解度变大
难度: 简单查看答案及解析
-
.实验室配制一定质量分数的稀硫酸并用其除铁锈,部分操作如图所示,其中正确的是( )
A.
量取浓硫酸 B.
 稀释浓硫酸
稀释浓硫酸C.
装生锈铁钉 D.
 倾倒稀硫酸
倾倒稀硫酸难度: 简单查看答案及解析
-
分析、推理和类比是化学学习中常用的思维方法,下列分析、推理或类比正确的是( )
A.物质与氧气发生的反应属于氧化反应,所以氧化反应一定有氧气参加
B.金刚石和石墨由于碳原子的排列方式不同,所以它们的物质性质存在很大的差异
C.无色酚酞溶液遇酸性溶液不变色,所以无色酚酞溶液不变色的一定是酸性溶液
D.碳酸盐能与盐酸反应生成气体,所以能与盐酸反应生成气体的一定是碳酸盐
难度: 中等查看答案及解析
-
浓硫酸与镁发生反应的化学反应方程式为:Mg+2H2SO4(浓)=MgSO4+X↑+2H2O,请根据该化学反应方程式判断以下说法,其中不正确的是( )
A. 反应后镁元素化合价升高了
B. X是SO2
C. 该反应说明浓H2SO4有脱水性
D. 反应后部分硫元素化合价发生了变化
难度: 简单查看答案及解析
-
甲、乙、丙三种固体物质(甲、乙、丙均不含结晶水)的溶解度曲线如图所示,下列说法不正确的是( )
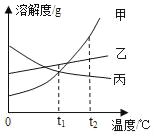
A. t1℃时,甲、丙两种物质的溶解度相等
B. t2℃时,将等质量的甲、乙、丙分别配成饱和溶液,所加水的质量:甲>乙>丙
C. 固体甲中含有少量杂质乙,可采用冷却热饱和溶液的方法提纯甲
D. t2℃时,将甲、乙、丙的饱和溶液分别降温至t1℃,所得溶液的溶质质量分数大小关系为:乙>甲>丙
难度: 中等查看答案及解析
-
下列除去杂质的方法中,合理的是( )
选项
物质
杂质
除杂方法
A
CO
CO2
通入足量的NaOH溶液后,干燥
B
NaCl溶液
NaOH
加入适量稀硫酸
C
铁粉
铜粉
加入足量稀硫酸,过滤
D
CaO
CaCO3
加入适量稀盐酸,过滤
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
在氯化亚铁和氯化铜的混合溶液中加入镁粉,下列说法不正确的是( )
A. 若反应完成后镁无剩余,溶液中若有Cu2+,一定有Mg2+和Fe2+
B. 若反应完成后镁无剩余,溶液中若无Cu2+,一定有Mg2+可能有Fe2+
C. 若反应完成后镁有剩余,则溶液中有Mg2+,无Cu2+,可能有Fe2+
D. 若反应完成后镁有剩余,则溶液中有Mg2+,没有Cu2+和Fe2+
难度: 中等查看答案及解析
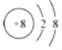 ,该微粒的符号是_____。
,该微粒的符号是_____。




