-
元素周期表是学习和研究化学的重要工具。如图是元素周期表的一部分,对相关信息表述正确的是
A. 氟原子的核内中子数为9
B. 氯原子的相对原子质量是
C. 氟、硫、氯三种元素的根本区别是质子数不同
D. 氟元素和氯元素位于元素周期表的同一周期
难度: 简单查看答案及解析
-
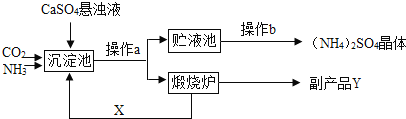
2016年,南京大学邹志刚课题组及其合作者利用ZnGa2O4介孔光催化材料用于CO2的光还原,成功实现了将CO2转化为碳氢化合物燃料。该反应化学方程式为CO2+2H2O
CH4+2O2.下列有关该反应说法错误的是( )
A. 此反应中碳元素化合价不变 B. 此反应前后分子个数不变
C. 此反应为
的利用创造一种新的方法 D. 此反应制取的
可以再生利用
难度: 简单查看答案及解析
-
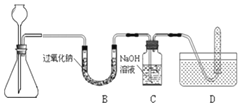
如图是碳和氧化铜在一定条件下进行反应的实验装置,该反应需几分钟时间。最能说明这个反应已经完成的实验现象是( )
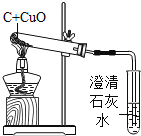
A. 装有澄清石灰水的试管中出现浑浊现象
B. 装有澄清石灰水的试管中不再有气泡冒出
C. 装有澄清石灰水的试管中不再出现浑浊现象
D. 装有氧化铜的试管中出现红色物质
难度: 简单查看答案及解析
-
地球上71%的面积覆盖着水,水是生命之源,也是重要的溶剂,下列说法正确的是( )
A. 只要是由水作溶剂形成的溶液,一定是无色透明的
B. 如果温度不变,水不蒸发,食盐溶液久置也不会析出食盐晶体
C. 将KC1、蔗糖溶于水后,溶质均以分子形式存在
D. 氢氧化钠固体溶解于水的过程中,既不放出热量,又不吸收热量
难度: 简单查看答案及解析
-
小兰用如图装置测定空气中氧气的体积分数时,发现进入集气瓶里的水的体积远大于集气瓶容积的
,针对这一事实,你认为可能的原因是( )
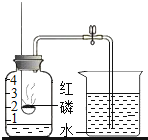
A. 没有预先检查装置气密性
B. 取用红磷的量太多
C. 实验时忘记事先夹紧止水夹
D. 实验后未等瓶内气体冷却,就打开止水夹
难度: 简单查看答案及解析
-
继黄金、白金之后,钯金(Pd)首饰在市场上悄然兴起。为了获得钯金,取17.7%的PdCl2溶液100g,加入10.0g铁粉使其充分反应得钯金和铁的氯化物。经分析所得钯金的质量为10.6g,未反应的铁粉质量为4.4g,下列说法正确的是( )
A. 生成铁的氯化物质量为
B. 生成铁的氯化物质量为
C. 该反应说明钯金比铁活泼 D. 生成铁的氯化物为
难度: 简单查看答案及解析