-
使用容量瓶配制溶液时,由于操作不当,会引起误差,下列情况会使所配溶液浓度偏低的是
①用天平(使用游码)称量时,被称量物与砝码的位置放颠倒了
②有些固体溶解会放热,若未经冷却即转移至容量瓶
③溶液转移到容量瓶后,烧杯及玻璃棒未用蒸馏水洗涤
④转移溶液前容量瓶内有少量蒸馏水
⑤定容时,仰视容量瓶的刻度线
⑥定容后摇匀,发现液面降低,又补加少量水,重新达到刻度线
A. ①③⑤⑥ B. ①②⑤⑥ C. ②③④⑥ D. ③④⑤⑥
难度: 简单查看答案及解析
-
实验室里需用480 mL 0.10 mol·L-1 CuSO4溶液,现选用500 mL容量瓶进行配制,以下操作正确的是
A. 称取7.68 g硫酸铜,加入500 mL水 B. 称取12.0 g胆矾配制500 mL溶液
C. 称取8.0 g硫酸铜,加入500 mL水 D. 称取12.5 g 胆矾配制500 mL溶液
难度: 简单查看答案及解析
-
现有一瓶乙二醇和丙三醇的混合物,已知它们的性质如表所示,据此将乙二醇和丙三醇互相分离的最佳方法是
物质
分子式
熔点(℃)
沸点(℃)
密度(g·cm-3)
溶解性
乙二醇
C2H6O2
-11.5
198
1.11
易溶于水和酒精
丙三醇
C3H8O3
17.9
290
1.26
能跟水、酒精以任意比互溶
A. 萃取法 B. 结晶法 C. 分液法 D. 蒸馏法
难度: 中等查看答案及解析
-
下列离子检验的方法正确的是
A. 向某溶液中加入硝酸银溶液,生成白色沉淀,说明原溶液中有Cl–
B. 向某溶液中加入氯化钡溶液,生成白色沉淀,说明原溶液中有SO42–
C. 向某溶液中加入氢氧化钠溶液,生成蓝色沉淀,说明原溶液中有Cu2+
D. 向某溶液中加入稀硫酸,生成无色气体,说明原溶液中有CO32–
难度: 简单查看答案及解析
-
科学家最近合成一种新型的氧分子O4,关于O4的下列说法,正确的是
A. 一个O4分子由两个O2分子构成 B. 是一种单质
C. 是一种化合物 D. 是一种混合物
难度: 简单查看答案及解析
-
根据溶解度曲线,在80 ℃时将含有等物质的量的硝酸钠和氯化钾混合溶液恒温蒸发,首先析出的是

A. 氯化钾 B. 硝酸钠
C. 氯化钠 D. 硝酸钾
难度: 中等查看答案及解析
-
下列现象与胶体的性质无关的是
A. 将盐卤或石膏加入豆浆,制成豆腐
B. 一枝钢笔使用两种不同型号的蓝黑墨水,易出现堵塞
C. 向FeCl3溶液中加入NaOH溶液,会出现红褐色沉淀
D. 清晨,人们经常看到阳光穿过茂密的树木枝叶所产生的美丽景象
难度: 中等查看答案及解析
-
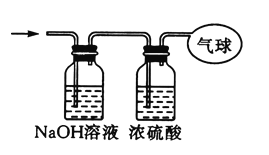
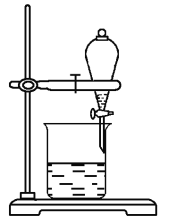
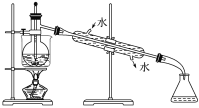
下列是一些装置气密性检查的方法,其中正确的是
A.
 B.
B.  C.
C.  D.
D. 
难度: 中等查看答案及解析
-
为了除去蛋白质溶液中混入的少量氯化钠,可以采用的方法是( )
A. 过滤 B. 电泳
C. 渗析 D. 加入AgNO3溶液,过滤
难度: 中等查看答案及解析
-
用如图表示的一些物质或概念间的从属关系中不正确的是( )
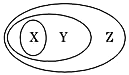
X
Y
Z
A
氧化物
化合物
纯净物
B
含氧酸
氧化物
化合物
C
胶体
分散系
混合物
D
碱性氧化物
金属氧化物
氧化物
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列溶液中c(Cl-)与50 mL 1 mol/L AlCl3溶液中c(Cl-)相等的是
A. 150 mL 1 mol/L的NaCl溶液 B. 75 mL 2 mol/L的NH4Cl溶液
C. 150 mL 2 mol/L的KCl溶液 D. 75 mL 1 mol/L的FeCl3溶液
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列叙述中不正确的是
A. 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA
B. 1.0L 1.0mo1·L-1的Na2CO3水溶液中含有的氧原子数为3 NA
C. 常温常压下,92g的NO2和N2O4混合气体含有的原子数为6NA
D. 1L 1.0mo1·L-1 NaOH溶液中含有OH一的数目为1 NA (忽略水的电离)
难度: 中等查看答案及解析
-
在无土栽培中,需配制一定量含50 mol NH4Cl,16 mol KCl和24 mol K2SO4的营养液。若用KCl、NH4Cl和(NH4)2SO4三种固体为原料来配制,三者的物质的量依次是(单位为mol)
A. 2 ,64 ,24 B. 64 ,2 ,24 C. 32 ,50 ,12 D. 16 ,50 ,24
难度: 简单查看答案及解析
-
在托盘天平的两盘上,分别放有两个质量相同的烧杯,各盛有6mol/L HCl 100mL,使天平达到平衡。分别向两烧杯中加入不超过5g的镁和铝,若要使其充分反应后天平仍保持平衡,则加入的镁与铝的质量之比为
A. 1:1 B. 24:27 C. 12:9 D. 32:33
难度: 中等查看答案及解析
-
某气体的摩尔质量为M g·mol-1,NA表示阿伏加德罗常数的值,在一定的温度和压强下,体积为V L的该气体所含有的分子数为X。则
表示的是
A. V L该气体的质量(以g为单位) B. 1 L该气体的质量(以g为单位)
C. 1 mol该气体的体积(以L为单位) D. 1 L该气体中所含的分子数
难度: 简单查看答案及解析
-
密度为0.91g/cm3的氨水,质量分数为25%.该氨水用等体积的水稀释后,所得溶液中溶质的质量分数( )
A. 等于12.5% B. 大于12.5%
C. 小于12.5% D. 无法确定
难度: 中等查看答案及解析
-
把500
有
和
的混合溶液分成5等份,取一份加入含
硫酸钠的溶液,恰好使钡离子完全沉淀;另取一份加入含
硝酸银的溶液,恰好使氯离子完全沉淀。则该混合溶液中钾离子浓度为
A.
B.
C.
D.
难度: 中等查看答案及解析
-
向量筒中注入水,仰视读数为a mL,倒出一部分水以后,俯视读数为b mL. ,则倒出水的实际体积为
A. (a-b) ml B. 大于(a-b) mL
C. 小于(a-b) mL D. 不能确定
难度: 简单查看答案及解析
-
己知FeO、Fe2O3、Fe3O4组成的混合物中,铁与氧的质量比为21:8,则混合物中FeO、Fe2O3、Fe3O4三种物质的物质的量之比为
A. 2:3:5 B. 1:1:33 C. 2:5:3 D. 1:2:3
难度: 中等查看答案及解析
-
t℃时,向xgKNO3不饱和溶液中,加入agKNO3或蒸发掉bg水恢复到t℃,溶液均达到饱和,据此下列推论错误的是
A. 在t℃时,KNO3的溶解度为100a/b g
B. 若原溶液中溶质质量分数为
,则x=2b
C. 若原不饱和溶液蒸发掉2b g水,恢复到原温度,能析出2a gKNO3
D. 在t℃时所配得的KNO3溶液中溶质质量分数≤
难度: 困难查看答案及解析