-
下列反应中属于中和反应的是( )
A. Zn+2HCl=ZnCl2+H2↑
B. CuO+2HCl=CuCl2+H2O
C. Ba(OH)2+H2SO4=BaSO4↓+2H2O
D. AgNO3+HCl=AgCl↓+HNO3
难度: 简单查看答案及解析
-
在试管中加入少量碘粒,再加入适量的汽油,振荡,静置,观察到的现象为( )

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
下列现有以下药品①苛性钠②醋酸 ③浓盐酸 ④浓硫酸 ⑤熟石灰,若未经密封保存,敞口放置一段时间后,质量增加并发生化学反应的是( )
A. ①③ B. ②④ C. ①⑤ D. ④⑤
难度: 中等查看答案及解析
-
部分食物和体液的近似pH如表所示.下列说法中正确的是( )
食物和体液
胃液
苹果汁
牛奶
血浆
pH
0.9~1.5
2.9~3.3
6.3~6.6
7.4~7.5
A.血浆和牛奶显碱性
B.胃液和苹果汁显酸性
C.胃液比苹果汁酸性弱
D.胃酸过多的人应多饮苹果汁
难度: 中等查看答案及解析
-
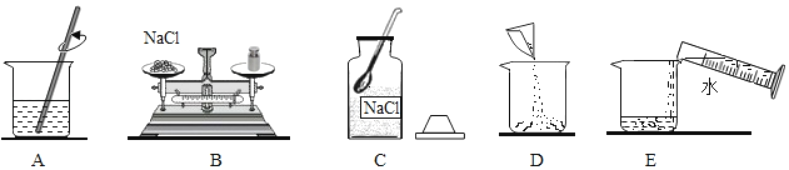
小明在实验操作技能考试中抽中的题目是“用固体氯化钠配制50g溶质质量分数为6%的氯化钠溶液”。他的有关做法正确的是( )
A. 选择的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、试剂瓶
B. 将氯化钠直接放在托盘天平左盘上称量3.0g
C. 用100 mL量筒量取所需水的体积
D. 用内壁附有水珠的烧杯配制溶液
难度: 简单查看答案及解析
-
打开啤酒瓶盖时,你会发现啤酒会自动喷出,喝了啤酒后又常常会打嗝,这说明气体溶解性与外界的压强和温度有关,下列关于气体溶解度说法不正确的是( )
A. 压强减少,气体溶解度增大
B. 压强减小,气体溶解度减小
C. 温度升高,气体溶解度减小
D. 温度降低,气体溶解度增大
难度: 简单查看答案及解析
-
类推是化学学习中常见的思维方法,以下类推正确的是( )
A. 活泼金属和酸反应有气体生成,所以与酸反应有气体生成的物质一定是活泼金属
B. 溶液具有均一性和稳定性,所以具有均一性和稳定性的液体一定是溶液
C. 碱的水溶液显碱性,所以NaOH的水溶液一定是碱性溶液
D. 酸与碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
难度: 中等查看答案及解析
-
将80g质量分数为35%的浓盐酸,稀释成14%的稀盐酸,需加水的质量为( )
A. 80g B. 100g C. 120g D. 200g
难度: 简单查看答案及解析
-
实验室配制一定溶质质量分数的食盐水,因疏忽导致所配溶液溶质质量分数偏低.分析以下原因,其中一定不会导致这种现象发生的是( )
A. 量取水时,仰视量筒的读数
B. 称量固体时,左盘放砝码,右盘放食盐
C. 配制溶液时,烧杯中原来留有水
D. 配制后的液体倾倒到细口瓶时,有一些液体溅出
难度: 简单查看答案及解析
-
下列物质的名称或俗称,指的不是同一种物质的是( )
A. 熟石灰 B. 氢氧化钙 C. 石灰石 D. 消石灰
难度: 简单查看答案及解析
-
如图所示,分别向试管内加入下列物质之一,能使U形管右侧液面显著升高的是( )

A. 浓盐酸 B. 浓硫酸 C. 食盐 D. 石灰石
难度: 中等查看答案及解析
-
如图所示,将水分别滴入装有氢氧化钠固体和硝酸铵固体的两支试管中,下列说法错误的是( )
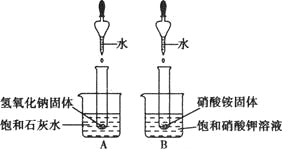
A. 硝酸铵固体溶解时会吸收热量
B. 氢氧化钠固体溶解时会放出热量
C. A、B两只烧杯的溶液中都有固体析出
D. A、B两只烧杯中溶液的溶质质量分数都保持不变
难度: 困难查看答案及解析
-
如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
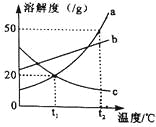
A. 随温度升高,a、b、c三种物质的溶解度均增大
B. t2℃时,把50g a放入50g水中,可得到100g a的饱和溶液
C. 将t2℃时等质量的a、b饱和溶液降温到t1℃,析出晶体的质量a大于b
D. t1℃时,a、c的溶解度相等,则两溶液的溶质质量分数也相等
难度: 中等查看答案及解析
-
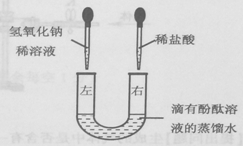
向滴有酚酞的盐酸溶液中逐滴加入氢氧化钠溶液,所得溶液的pH与加入溶液体积关系如图所示。下列说法正确的是( )
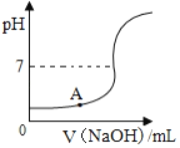
A. 反应过程中溶液温度降低
B. A点对应溶液的溶质为NaOH、NaCl
C. 恰好完全反应时溶液显中性
D. 反应过程中溶液的颜色由红色变为无色
难度: 简单查看答案及解析