-
3月22日是 “世界水日”。下列跟水有关的变化中没有化学变化的是( )
A. 海水晒盐 B. 太阳能光解水制氢气
C. 自来水生产 D. 肥皂水区分硬水和软水
难度: 中等查看答案及解析
-
下列归纳和总结完全正确的一组是( )
A.化学与生活
①用洗涤剂因为溶解性去除油污
②用镶有金刚石的玻璃刀裁玻璃
③用生石灰作食品干燥剂且发生放热现象
B.化学与安全
①炒菜锅着火可以用锅盖盖灭
②在室内一盆水能防止煤气中毒
③夜间发现液化气泄漏开灯寻找泄漏源
C.化学与资源
①防止金属腐蚀是保护金属资源的途径之
②煤、石油、天然气是不可再生能源
③海洋中蕴藏着丰富的化学资源
D.化学与发现
①波义耳发现酸碱指示剂
②拉瓦锡发现元素周期律并编制元素周期表
③门捷列夫发现空气的组成
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
化学是以实验为基础的学科,下列有关实验现象的描述正确的是( )
A. 电解水实验中正极与负极产生的气体体积之比为 1:8
B. 打开浓盐酸的瓶塞会看到白烟,而打开浓硫酸瓶塞无明显现象
C. 硫粉在氧气中燃烧产生蓝紫色火焰
D. 在氯化铜溶液中加入锡片,析出红色固体铜单质
难度: 中等查看答案及解析
-
某同学化学笔记本上有如下记录,你认为正确的是( )
A. 用钛和钛合金打造的轮船部件使用一段时间后仍然光亮如初,是因为它具有形状记忆功能
B. 生铁、钢、黄铜、硬铝、氧化铁等均属于合金
C. Na和Na+都是钠元素,它们的化学性质相同
D. 二氧化碳、甲烷、臭氧都能引起温室效应
难度: 困难查看答案及解析
-
从下列图片中不能获取的信息是( )
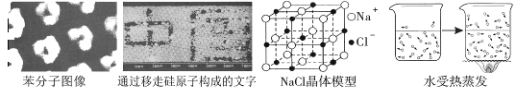
A. 分子之间有间隔 B. 受热水分子运动速率加快
C. 硅原子是由原子核和电子构成的 D. 构成物质的粒子有分子、原子和离子
难度: 中等查看答案及解析
-
下列各组物质按单质、化合物和混合物顺序排列的是( )
A. 冰、生石灰、天然气 B. 金刚石、高锰酸钾、石油
C. 液态载、碘酒、生理盐水 D. 甲烷、盐酸、酒精
难度: 中等查看答案及解析
-
甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示:根据以上微观 示意图得出的结论中.正确的是( )
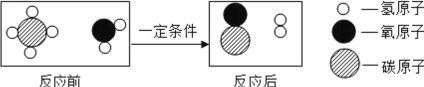
A. 该反应属于置换反应
B. 水煤气的成分是一氧化碳和氧气
C. 该反应中含氢元素的化合物有3种
D. 该反应的化学方程式中甲烷和水的计量数之比为1:1
难度: 中等查看答案及解析
-
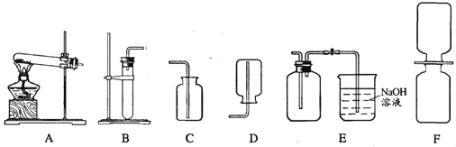
下列装置所示的实验中,能达到实验目的是 ( )
A.
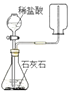 制取并收集CO 2 B.
制取并收集CO 2 B. 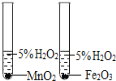 比较MnO 2和Fe 2O3的催化效果
比较MnO 2和Fe 2O3的催化效果C.
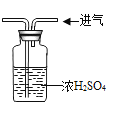 干燥氢气 D.
干燥氢气 D. 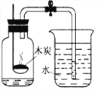 测空气中O2的含量
测空气中O2的含量难度: 困难查看答案及解析
-
下列关于溶液、悬浊液、乳浊液的说法:
①溶液一定是无色、均一、稳定、透明的液体;②溶液中溶质可以有多种,但溶剂只有一种;③溶液是纯净物,而浊液是混合物;④酸溶液呈酸性,呈酸性的一定是酸溶液;⑤植物油与水形成乳浊液,泥水是悬浊液;⑥饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液。其中正确的个数有
A. 2 B. 3 C. 4 D. 5
难度: 困难查看答案及解析
-
关于溶液配制过程中遇到的问题,下列做法或说法正确的是( )
A. 用天平称量溶质时,出现了右盘低的现象,接下来应该减小右盘中砝码
B. 用浓硫酸配制稀硫酸,应将水慢慢倒入装有浓硫酸的量筒中
C. 若其他操作正确,量取溶剂时俯视读数,则所配溶液的溶质质量分数偏小
D. 25g的胆矾全部溶于75g水中,能形成溶质质量分数为16%的硫酸铜溶液
难度: 困难查看答案及解析
-
下列有关量的变化图象与其对应叙述相符的是( )
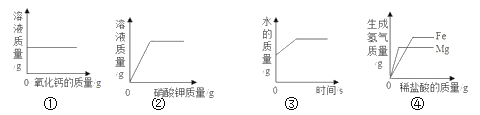
A. ①常温下,向一定量的饱和石灰水中加入氧化钙
B. ②一定温度下,向不饱和硝酸钾溶液中加入硝酸钾
C. ③向一定质量的过氧化氢的水溶液中加入二氧化锰
D. ④向等质量的铁和镁中分别加入足量的稀盐酸
难度: 困难查看答案及解析
-
下列“家庭小实验”不能达到预期目的的是( )
A. 用可乐、芬达、雪碧等汽水制二氧化碳
B. 用空塑料瓶、小卵石、石英沙、活性炭、膨松棉等制作简易净水器
C. 向洗净的碎鸡蛋壳中加入食盐水可制二氧化碳
D. 用酒精浸泡捣烂的某些植物的花瓣可制酸碱指示剂
难度: 中等查看答案及解析
-
图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
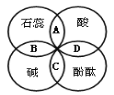
A. 紫色 B. 蓝色 C. 红色 D. 无色
难度: 简单查看答案及解析
-
产生下列现象,只与空气中的水蒸气有关的是( )
A. 铜制品长期放在空气中会产生“铜锈”[又称“铜绿”,化学式为Cu2(OH)2CO3]
B. 浓硫酸露置于空气中会增重、变稀
C. 浓盐酸露置于空气中会变轻、变稀
D. 铁粉可以作为食品的“双吸剂”
难度: 中等查看答案及解析
-
除去下列各组物质中的杂质(括号内为杂质),所选用的试剂(足量)及操作方法均正确的是( )
选项
物质
选用试剂
操作方法
A
Fe(Cu)
盐酸
浸泡、过滤、洗涤、烘干
B
CO(CO2)
NaOH溶液、浓硫酸
洗气、干燥
C
CaO(CaCO3)
水
过滤、烘干
D
KCl(MnO2)
水
溶解、蒸发结晶
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
往AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,待反应完成后再过滤,不可能存在的情况是( )
A. 滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Fe2+
B. 滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+
C. 滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+
D. 滤纸上有Ag、Cu、Fe,滤液中有Zn2+、Fe2+、Cu2+
难度: 困难查看答案及解析
-
KNO3的溶解度如表,下列说法错误的是
温度/℃
0
20
40
60
80
100
溶解度/g
13.3
31.6
63.9
110
169
246
A. 硝酸钾的溶解度受温度影响变化较大
B. 60 ℃时,饱和硝酸钾溶液中溶质与溶液质量之比为11∶21
C. 20 ℃时,10 g水中加入5 g硝酸钾充分溶解后再加入5 g水,前后溶质的质量分数不变
D. 将溶质质量分数为28%的硝酸钾溶液从60 ℃降温至20 ℃,没有晶体析出
难度: 中等查看答案及解析
-
如图为某固体溶解度随温度变化的曲线。该固体从溶液中析出时不带结晶水。M、N两点分别表示该固体形成的两份溶液在不同温度时的浓度。当条件改变时,溶液新的状态在图中对应的点的位置可能也随之变化,其中判断不正确的( )
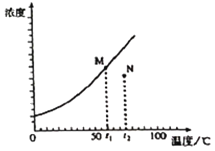
A. 都升温10℃后,M、N点均向右平移
B. 加溶质(温度都不变)时,M点均不动,N点上移
C. 都降温10℃后,M点沿曲线向左下移,N点向左平移
D. 蒸发溶剂(假设温度都不变)时,先是M点不动,N点左平移至曲线;继续蒸发溶剂,M、N点都不动
难度: 中等查看答案及解析
-
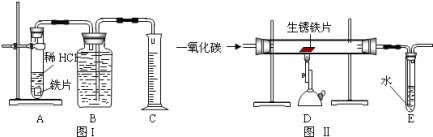
为探究锌、铜、铁三种金属的活动性顺序,某学习小组做了如甲图所示实验,实验结束后,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如乙图所示),下列说法正确的是( )
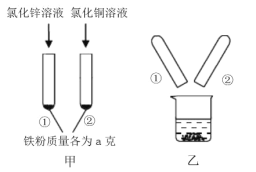
A. 反应后乙烧杯中的固体一定含有铁
B. 甲图试管②中反应后固体一定不含铁
C. 反应后烧杯中的溶液一定不含有氯化铜
D. 烧杯中最后所得固体的质量一定小于 2a 克
难度: 困难查看答案及解析