-
对下列物质的俗称,理解错误的是( )
A. 干冰不是冰 B. 纯碱不是碱 C. 水银不是银 D. 醋酸不是酸
难度: 简单查看答案及解析
-
1869年,( )发现了元素周期律并编排了元素周期表。
A. 波义耳 B. 拉瓦锡 C. 道尔顿 D. 门捷列夫
难度: 简单查看答案及解析
-
吸烟有害健康,烟气中的一种有毒气体是( )
A. O2 B. CO C. SO2 D. CO2
难度: 简单查看答案及解析
-
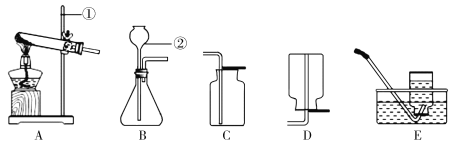
下列实验操作正确的是 ( )
A.
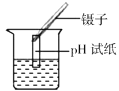 测定溶液酸碱度 B.
测定溶液酸碱度 B. 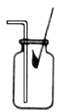 验满氧气
验满氧气C.
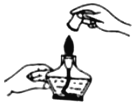 熄灭酒精灯 D.
熄灭酒精灯 D. 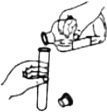 倾倒液体
倾倒液体难度: 中等查看答案及解析
-
材料对我们的生活影响越来越大,钛合金属于( )
A. 金属材料 B. 合成材料 C. 复合材料 D. 天然材料
难度: 中等查看答案及解析
-
下列含氮物质中,氮元素化合价最低的是( )
A. NH3·H2O B. N2 C. HNO3 D. NO
难度: 简单查看答案及解析
-
下列有关物质燃烧现象的叙述中,正确的是( )
A. 硫粉在氧气中燃烧时,产生淡蓝色火焰,生成一种刺激性气味的气体
B. 红磷在空气中燃烧时,产生大量白色烟雾
C. 木炭在氧气中燃烧时,发出白光,生成无色无味的气体
D. 棉线在空气中燃烧时,有烧焦羽毛的气味
难度: 中等查看答案及解析
-
下列关系曲线不能正确反映其对应变化关系的是( )
A.
加热KClO3和MnO2固体混合物
B.
向Ca(OH)2溶液中通入CO2至过量
C.
向一定浓度的NaOH溶液中加水稀释
D.
 将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al
将等质量的Mg和Al分别与过量等浓度的盐酸反应,则a为Mg,b为Al难度: 中等查看答案及解析
-
某无色溶液中大量存在的离子如图所示,其中X可能是( )
A. H+ B. Cu2+ C. NH4+ D. K+
难度: 简单查看答案及解析
-
蛋白质是人类重要的营养物质,通过食物获得的蛋白质,在胃肠道里与水反应生成丙氨酸(C3H7O2N)等氨基酸。下列说法不正确的是( )
A. 蛋白质属于有机高分子化合物
B. 丙氨酸中氮元素的质量分数约为15.7%
C. 1个丙氨酸分子中含有一个氧分子
D. 丙氨酸中碳元素和氧元素质量比为9:8
难度: 简单查看答案及解析
-
如图是氢氧化钠溶液与稀盐酸反应的微观示意图,下列有关该图示的说法正确的是( )

A. 反应前后,溶液的pH不变
B. 向反应后溶液中滴加酚酞,溶液呈红色
C. 该图表示氢氧化钠和盐酸恰好完全反应
D. 该反应实质是Na+和Cl-结合生成NaCl
难度: 中等查看答案及解析
-
茶氨酸(C7H14O3N2)具有降低血压、提高记忆力、保护神经细胞、减肥等功效。下列有关说法正确的是
A.茶氨酸属于有机化合物 B.茶氨酸中氧元素的质量分数最大
C.茶氨酸由26个原子构成 D.茶氨酸中碳、氢、氧、氮各元素的质量比为7:14:3:2
难度: 中等查看答案及解析
-
除去下列物质中的少量杂质(括号内为杂质),拟定的实验方案可行的是( )
A. NaOH溶液(Na2CO3):加入适量的BaCl2溶液至恰好完全反应,过滤
B. 二氧化碳(氯化氢气体):依次通过足量的氢氧化钠溶液和浓硫酸
C. MnO2固体(KCl):加入适量水溶解,过滤,蒸发
D. 氧气(水蒸气):通过装有足量无水氯化钙的干燥管
难度: 简单查看答案及解析
-
在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列说法不正确的是( )
物质
a
b
c
d
反应前的质量/g
30
20
10
15
反应后的质量/g
x
y
0
10
A. 参加反应的c与d质量之比是2:1 B. x的取值范围是:0≤x≤30
C. 当y≤20时,该反应是化合反应 D. x+y=65
难度: 中等查看答案及解析