-
下列物质中,不属于“空气污染物”的是( )
A. PM2.5 B. 二氧化氮 C. 二氧化碳 D. 二氧化硫
难度: 简单查看答案及解析
-
下列属于物质物理性质的是( )
A. 氧化性 B. 导热性 C. 助燃性 D. 还原性
难度: 简单查看答案及解析
-
下列化学用语正确的是( )
A. 小苏打﹣Na2CO3 B. 铝离子﹣Al2+
C. 二氧化氯﹣ClO2 D. 氯酸钾﹣KCl
难度: 中等查看答案及解析
-
下列做法错误的是( )
A. 秸秆粉粹,获得肥料 B. 共享单车,节能减排
C. 油锅着火,加水浇灭 D. 煤气泄漏,关阀开窗
难度: 中等查看答案及解析
-
下列归类错误的是( )
选 项
归 类
内 容
A
化石燃料
煤、石油、天然气
B
常见合金
黄铜、硬铝、玻璃钢
C
同一物质
烧碱、火碱、苛性钠
D
糖类物质
淀粉、蔗糖、纤维素
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列实验设计错误的是 ( )
A. 用托盘天平称取6.4g食盐
B. 用碘酒区分葡萄糖和淀粉
C. 用Na2CO3溶液除去H2中的HCl
D. 用湿润的红色石蕊试纸检验NH3
难度: 中等查看答案及解析
-
下列排序正确的是
A. 地壳中元素的含量:
B. 金属材料的熔点:
C. 金属活动性顺序:
D. 氯元素的质量分数:
难度: 中等查看答案及解析
-
下列对实验现象的描述或实验操作正确的是( )
A. 细铁丝在空气中燃烧,火星四射
B. 饱和澄清石灰水升温后会变浑浊
C. 鸡蛋清中滴加饱和硫酸铵溶液,出现黄色固体
D. 蒸发食盐水时,将蒸发皿中水分蒸干后停止加热
难度: 中等查看答案及解析
-
以甲为原料得到丙反应的微观过程如下:

下列说法正确的是
A. 该反应为置换反应 B. 转化中甲和乙的分子个数之比为1∶1
C. 甲中氧元素的质量分数大于丙 D. 反应中一定有元素化合价发生改变
难度: 中等查看答案及解析
-
下列指定反应的化学方程式正确的是
A. 《天工开物》烧石灰:CaCO3
CaO + CO2↑
B. 乙炔的完全燃烧:C2H2 + O2
H2O + 2CO2
C. 稀硫酸除铁锈:2H2SO4 + Fe2O3=2FeSO4+2H2O
D. 铜生锈形成铜绿:2CuO + H2O + CO2=Cu2(OH)2 CO3
难度: 中等查看答案及解析
-
物质性质决定用途。下列说法错误的是( )
A. 洗涤剂有乳化作用,可用来清洗油污
B. 氮气化学性质稳定,可用作灯泡的填充气
C. 二氧化碳能溶于水且与水反应,可制碳酸饮料
D. 烧碱能与酸反应,可用于消除面团发酵产生的酸味
难度: 中等查看答案及解析
-
下列物质的转化在给定条件下均能实现的是
A. O2
CO2
CO B. BaCl2溶液
BaCO3
Ba(OH)2
C. SO2
H2SO4
Fe2(SO4)3 D. CuSO4
Cu(OH)2
 CuO
CuO难度: 简单查看答案及解析
-
下列实验操作中(括号内为杂质或待检验物质)不能达到实验目的是( )
选项
物质
目的
主要实验操作
A
牛奶、米汤
鉴别
取样,灼烧,闻气味
B
Na2CO3(NaOH)溶液
检验
滴加酚酞试液,观察溶液颜色变化
C
KCl(KClO3)固体
除杂
加热至固体质量不变
D
CaCO3、CaCl2固体
分离
溶解、过滤、洗涤、干燥、蒸发
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
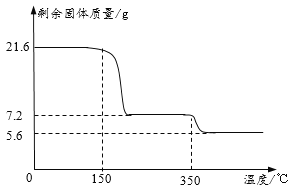
已知:Mg(OH)2
MgO+H2O.一定质量的Mg(OH)2和MgO的混合物加热一段时间后,将生成的气体通入到浓硫酸中,增重1.8g,已知剩余固体的质量为13.8g,剩余固体中Mg元素的质量为7.2g,下列说法错误的是( )
A. 剩余固体为混合物
B. 原混合物中Mg元素的质量为7.2g
C. 混合物中Mg(OH)2与MgO的质量之比为29:20
D. 加热前后的固体分别与相同浓度稀盐酸恰好完全反应所消耗盐酸质量相等
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. 向NaOH固体中加入稀盐酸温度升高,说明该反应放热
B. 某化肥与熟石灰研磨,无刺激性气味,说明化肥一定不是氮肥
C. 在酒精灯上加热铝箔,铝箔熔化但不滴落,说明氧化铝的熔点比铝高
D. 向黑色粉末中加入一种液体,立即产生大量气泡,说明该液体一定是双氧水
难度: 中等查看答案及解析
-
NH4Cl和Na2SO4的溶解度表及溶解度曲线如下。下列说法正确的是
温度/℃
10
20
30
40
50
60
溶解度
S/g
NH4Cl
33.3
37.2
41.4
45.8
50.4
60.2
Na2SO4
9.6
20.2
40.8
48.4
47.5
47.0

A. 甲为NH4Cl
B. t3℃应介于30℃~40℃
C. 乙物质的饱和溶液从t2升温到t3,溶液的溶质质量分数不变
D. 甲、乙饱和溶液从t3降温到t1,析出晶体(均不带结晶水)的质量一定相等
难度: 中等查看答案及解析
-
将稀盐酸逐滴匀速加入到一定量的稀氢氧化钠的溶液中,用数字化仪器对反应过程中溶液的温度、pH进行实时测定,得到的曲线如图所示。
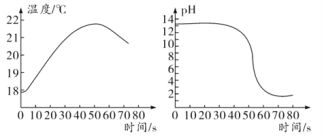
基于证据推理不正确的是
A. 根据pH减小且低于7的事实,可以判断稀盐酸与稀氢氧化钠发生了化学反应
B. 该反应大约在60 s时恰好完全反应
C. 反应体系温度升高,是否为稀盐酸或稀氢氧化钠溶液被稀释所导致,还需要通过实验证明
D. 对于“无明显现象的化学反应”还可以通过检测反应物的消失或新物质的生成来进行验证
难度: 中等查看答案及解析
 读取液体体积 B.
读取液体体积 B. 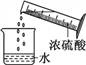 稀释浓硫酸
稀释浓硫酸 制取氢气 D.
制取氢气 D.  检验氢气纯度
检验氢气纯度