-
往AgNO3和Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤渣中加入稀盐酸,无气泡产生。根据上述现象,你能得出的结论是 ( )
A. 滤渣中一定有Fe粉 B. 滤渣中一定有Cu粉
C. 滤液中一定有Fe2+ D. 滤液中一定有Ag+、Cu 2+
难度: 中等查看答案及解析
-
物质的性质决定物质的用途,下列物质的用途中利用其化学性质的是( )
①天然气用作燃料;②氦气用作填充探空气球;③氧气用于急救病人; ④干冰用作人工降雨; ⑤焦炭用于冶炼金属
A. ①③⑤ B. ①②③ C. ③④⑤ D. ①④⑤
难度: 简单查看答案及解析
-
生活中常见的下列物质属于纯净物的是( )
A. 消毒酒精 B. 冰水混合体 C. 不锈钢 D. .食醋
难度: 简单查看答案及解析
-
党的十八大报告中把“生态文明建设”首次提升到更高的战略层面,要求加大自然生态系统和环境保护力度.下列做法不符合这一要求的是( )
A. 合理开发洁净能源
B. 全面关停化工企业
C. 改进汽车尾气净化技术
D. 研发易降解的生物农药和塑料
难度: 中等查看答案及解析
-
根据所学过的化学知识,判断下列说法错误的是( )
A. 体温计中的水银不是银,而是金属汞
B. 蒸馒头用的纯碱不是盐,而是碱
C. 合金不是合成材料,而是金属材料
D. 白金不是金,而是铂
难度: 简单查看答案及解析
-
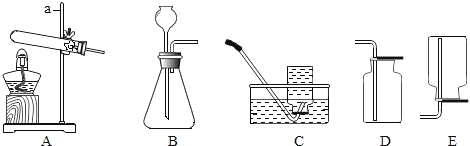
下列实验操作正确的是( )
A.
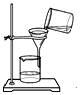 过滤 B.
过滤 B. 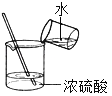 稀释浓硫酸
稀释浓硫酸C.
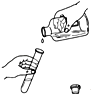 倾倒液体 D.
倾倒液体 D.  闻气味
闻气味难度: 简单查看答案及解析
-
根据如图提供的信息,下列说法正确的是( )
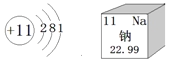
A. 钠属于非金属元素
B. 钠的相对原子质量是22.99g
C. 钠离子最外层有1个电子
D. 钠的原子序数为11
难度: 中等查看答案及解析
-
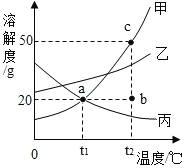
某溶液的溶质质量分数为20%,加入50g水后变为10%,则原溶液的质量为( )
A. 100g B. 50g C. 150g D. 200g
难度: 简单查看答案及解析
-
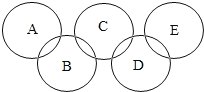
下列四种物质中,有一种和其他三种物质都能发生反应的是( )
A. 硝酸银溶液 B. 石灰石 C. 稀盐酸 D. 烧碱
难度: 中等查看答案及解析
-
有四种物质的溶液:①Ba(OH)2②Na2SO4③HCl ④FeCl3,不用其他试剂就可以将它们逐一鉴别出来,其鉴别的顺序是( )
A. ④③②① B. ④①②③ C. ①③④② D. ①④②③
难度: 中等查看答案及解析
-
3月23至25日,佛山展开了“功勋航天员走进校园”活动,学生知道了很多飞船的知识.飞船常利用反应2Na2O2+2CO2=2X+O2来提供氧气,“X”中物质的化学式是( )
A. CO B. Na2O C. NaOH D. Na2CO3
难度: 中等查看答案及解析
-
下列物质中,属于氧化物的是( )
A. 氧气 B. 熟石灰
C. 干冰 D. 过氧化氢溶液
难度: 简单查看答案及解析
-
下列依据实验目的进行的实验设计,合理的是( )
实验目的
实验设计
A
从空气中获取纯净的氮气
用硫燃烧除去空气中的氧气
B
区别硝酸铵和氢氧化钠固体
加适量的水溶解,测量前后温度变化
C
除去混在二氧化碳中的氯化氢气体
把混合气体通过足量的氢氧化钠溶液
D
检验某物质中是否含有SO42﹣
取样溶解,滴加BaCl2溶液和稀硝酸
A. A B. B C. C D. D
难度: 中等查看答案及解析