-
从化学的角度对下列诗句、成语等进行解释,其中不正确的是( )
A. “遥知不是雪,为有暗香来”﹣﹣分子在不停地运动
B. “点石成金”﹣﹣化学反应改变了元素种类
C. “真金不怕火炼”﹣﹣金(Au)的化学性质不活泼
D. “釜底抽薪”(釜:烹煮食物的容器.薪:柴禾)﹣﹣破坏了燃烧的条件
难度: 简单查看答案及解析
-
下列说法错误的是( )
A. 饱和溶液一定是浓溶液
B. 糖水、汽水都是溶液
C. 洗洁精去油污是因为洗洁精具有乳化功能
D. 溶液都是均一、稳定的混合物
难度: 中等查看答案及解析
-
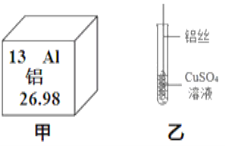
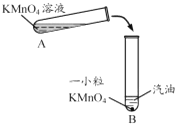
能验证 Zn、Cu、Ag 三种金属活动性顺序的一组试剂是
A. Zn、Ag、CuSO4溶液
B. Zn、Cu、Ag、H2SO4溶液
C. Cu、Ag、ZnSO4溶液
D. Ag、ZnSO4溶液、CuSO4溶液
难度: 中等查看答案及解析
-
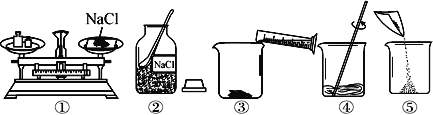
实验室配制溶质质量分数为
的氯化钠溶液50g,下列操作正确的是
A.
 取氯化钠 B.
取氯化钠 B. 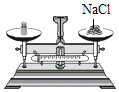 称氯化钠
称氯化钠C.
量取水 D.
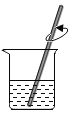 溶解
溶解难度: 简单查看答案及解析
-
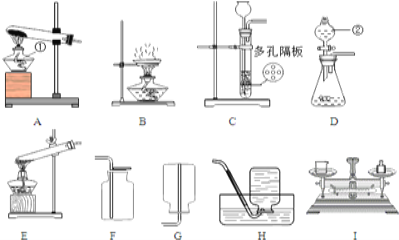
设计对比实验,控制变量是学习化学的重要方法,下列对比实验不能达到目的是( )
编号
A
B
C
D
实验设计
实验目的
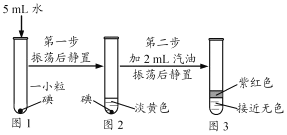
探究同种物质在不同溶剂中的溶解性
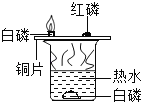
探究物质燃烧的条件
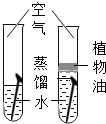
探究铁生锈的条件
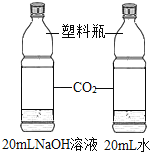
探究CO2与NaOH溶液能否发生反应
A. A B. B C. C D. D
难度: 困难查看答案及解析
-
推理是化学学习中常用的思维方法,下列推理正确的是( )
A. 溶液是均一稳定的,所以均一稳定的物质一定是溶液
B. 溶液中无固体剩余时,该溶液一定是不饱和溶液
C. 点燃可燃性气体前要验纯,所以点燃氢气前一定要验纯
D. 化学变化伴随着能量的变化,则有能量变化的一定是化学变化
难度: 中等查看答案及解析
-
向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
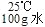
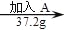 ①
①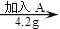 ②
②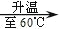 ③
③ ④
④ ⑤
⑤资料:A的溶解度
温度/℃
20
30
40
50
60
溶解度/g
37.2
41.4
45.8
50.4
55.2
A. ②中A的质量分数最大 B. ③⑤中A的质量分数相等
C. ②④⑤的溶液为饱和溶液 D. ①③④⑤中没有固体存在
难度: 困难查看答案及解析
-
如图是固体物质M的溶解度曲线,下列说法正确的是

A. 40℃时,其饱和溶液中溶质的质量分数为50%
B. M的溶解度随温度升高而一直增大
C. 将40℃是M的饱和溶液降温至10℃,有固体析出
D. 将50℃时M的饱和溶液升温至80℃,溶液变为不饱和溶液
难度: 中等查看答案及解析
-
右图为甲、乙两种固体物质的溶解度曲线,下列叙述不正确的是
 A.甲、乙两种物质均属于易溶物质
A.甲、乙两种物质均属于易溶物质B.甲物质的溶液度受温度变化的影响较大
C.在20℃时,甲、乙两种物质的饱和溶液中溶质的质量相等
D.当甲中含有少量的乙时,可用降温结晶法提纯甲
难度: 简单查看答案及解析
-
下图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是( )
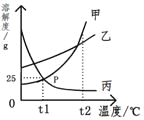
A. t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4
B. P点表示甲、丙两种物质的饱和溶液质量相等
C. t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液
D. 将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质
难度: 困难查看答案及解析