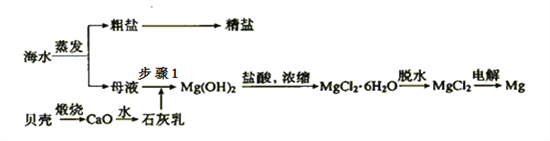
-
已知①2Fe3++ Fe ===3Fe2+②2Fe2++Cl2 ===2Fe3++2Cl- ,以下说法正确的是( )
A. 氧化性由强到弱的顺序是:Cl2>Fe3+ >Fe2+
B. ①中氧化产物与还原产物之比是2:1
C. Fe2+ 在①中仅为氧化产物,Fe2+在②中为还原剂
D. ②中有1molCl2发生反应时,转移1mol的电子
难度: 中等查看答案及解析
-
我国宋代沈括在《梦溪笔谈》中记载:“信州铅山县有苦泉,流以为涧。挹其水熬之,则成胆矾。熬胆矾铁釜,久之亦化为铜。”下列对文中加点词语的理解,正确的是
A. “苦泉”中泉水属于胶体 B. “熬”表示加热蒸馏
C. “胆矾”化学式为CuSO4 D. “化”表示置换转化
难度: 中等查看答案及解析
-
分类法在化学的发展中起到非常重要的作用,下列分类标准合理的是
①根据氧化物的组成元素将氧化物分成酸性氧化物碱性氧化物和两性氧化物
②根据反应中是否有化合价变化将化学反应分为氧化还原反应和非氧化还原反应
③根据分散系是否有丁达尔效应将分散系分为溶液胶体和浊液
④根据反应中的热效应将化学反应分为放热和吸热反应
⑤根据水溶液能否导电将化合物分为电解质和非电解质
A. ②④ B. ②③④ C. ①③⑤ D. ⑤④①②
难度: 中等查看答案及解析
-
现有①MgSO4 ②Ba(NO3)2 ③NaOH ④CuCl2四种溶液,不加其他试剂就可鉴别出来,鉴别的先后顺序是( )
A. ④③①② B. ③④①② C. ②①③④ D. ③④②①
难度: 中等查看答案及解析
-
下列反应的离子方程式不正确的是
A. 铁与稀盐酸反应:2Fe + 6H+ =2Fe3 ++ 3H2↑
B. 氢氧化钠溶液与盐酸反应:OH—+ H+ = H2O
C. 锌与硫酸铜溶液反应:Zn + Cu2+ = Zn2+ + Cu
D. 氯化钡溶液与稀硫酸反应:Ba2+ + SO42- = BaSO4↓
难度: 中等查看答案及解析
-
下列离子在溶液中能共存,加 OH-有沉淀析出,加 H+能放出气体的是( )
A. Na+、Cu2+、Cl-、SO42- B. Ba2+、K+、Cl-、NO3-
C. Ba2+、NH4+、CO32-、NO3- D. Na+、Ca2+、Cl-、HCO3-
难度: 中等查看答案及解析
-
24mL浓度为0.05mol·L-1的Na2SO3溶液恰好与20mL浓度为0.02mol·L-1的K2Cr2O7溶液完全反应。已知亚硫酸钠被氧化为硫酸钠,则铬元素在还原产物中的化合价为( )
A. +3价 B. +4价 C. +5价 D. +6价
难度: 中等查看答案及解析
-
下列反应中,水既不是氧化剂也不是还原剂的氧化还原反应是
A. C + H2O
CO + H2 B. 2H2O+2Na=2NaOH+H2↑
C. Cl2 + H2O
HCl + HClO D. SO3 + H2O=H2SO4
难度: 简单查看答案及解析
-
下列转化过程中必须加入还原剂的是
A. KClO3→KCl B. SO2→SO32- C. Fe3+→Fe2+ D. Cu→Cu2+
难度: 简单查看答案及解析
-
有些离子方程式能表示一类反应,有些离子方程式却只能表示一个反应。下列离子方程式中,只能表示一个化学反应的是( )
A. OH-+HCO3—===CO32—+H2O B. Cl2+H2O
H++Cl-+HClO
C. CO32—+2H+===CO2↑+H2O D. Ag+Cl-===AgCl↓
难度: 中等查看答案及解析
-
在反应3Cl2+6KOH(浓)
KClO3+5KCl+3H2O中,氧化剂与还原剂的物质的量之比为
A. 5:1 B. 4:1 C. 1:5 D. 1:4
难度: 中等查看答案及解析
-
下列有关实验的操作正确的是
选项
实验
操作
A
制备Fe(OH)3胶体
煮沸盛在小烧杯中的25mL蒸馏水,加入5~6滴饱和FeCl3溶液,继续煮沸至红褐色,即停止加热。
B
配制250mL0.1mol/L氢氧化钠溶液
称取1.0gNaOH固体放入250mL容量瓶中,加水至离刻度线1~2cm处,改用胶头滴管滴入蒸馏水到刻度
C
氢气还原氧化铜
用酒精灯加热盛有灼热的氧化铜的反应管并通入氢气,固体完全变红后,先停止通氢气,然后停止加热
D
除去NaBr溶液中少量的NaI
在溶液中滴入少量AgNO3溶液至不再产生黄色沉淀,然后过滤
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
用红色激光照射下列物质,能观察到丁达尔效应的是
A. 乙醇溶液 B. 牛奶 C. 硫酸铜溶液 D. 蔗糖溶液
难度: 简单查看答案及解析
-
2克氧气含有x个氧分子,则阿伏加德罗常数为
A. 16x B. 32x C. x/16 D. x
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值,下列叙述正确的是
A. 常温常压下,20g氖气所含有的原子数目为0.5NA
B. 2.8铁粉与50mL4 mol·L-1盐酸完全反应转移电子的数目为0.1NA
C. 标准状况下,22.4 LSO2和SO3混合物中含有的硫原子数目为0.1NA
D. 28g的C2H4和N2混合气体中含有的原子数为2NA
难度: 中等查看答案及解析
-
(题文)在同温同压下,向大小相同的气球分别充入CO和以下四种混合气体,当体积相等时A、B、C、D四个气球内,与充入CO气球内所含原子数一定相等的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
实验室用质量分数为98%、ρ=1.84 g·mL-1的浓硫酸配制190 mL 1.0 mol·L-1的稀硫酸,下列说法正确的是
A. 所用浓硫酸的物质的量浓度为9.2 mol·L-1
B. 所用容量瓶的规格为190 mL
C. 需用15 mL量筒量取10.3 mL浓硫酸
D. 定容时俯视容量瓶刻度,导致所配溶液浓度偏高
难度: 困难查看答案及解析
-
用NA表示阿伏加德罗常数的值。下列判断错误的是( )
A. NA个H+的质量为1 g
B. 2 L 0.5 mol/L Na2SO4溶液中含NA个Na+
C. 32 g O2中含有2NA个氧原子
D. 标准状况下,1 mol H2O中含有NA个分子
难度: 中等查看答案及解析
-
在0.1 L由NaCl、MgCl2、BaCl2组成的混合溶液中,部分离子浓度大小如图所示,下列对该溶液成分说法不正确的是( )

A. NaCl的物质的量为0.1mol
B. 该混合液中BaCl2的物质的量为0.05mol
C. 溶质MgCl2的质量为9.5 g
D. 将该混合液加水稀释至体积为1 L,稀释后溶液中的Na+物质的量的浓度为0.1mol/L
难度: 简单查看答案及解析