-
溶液是一种重要的混合物。下列有关溶液的说法正确的是( )
A. 溶液具有均一性和稳定性,因为溶液中的各种粒子保持静止不动
B. 饱和溶液是一定温度下不能再溶解该物质的溶液
C. 不饱和溶液通过降低温度一定能变成饱和溶液
D. 一种物质分散到另一种物质里一定能形成溶液
难度: 中等查看答案及解析
-
下列各组物质的溶液不用其他试剂无法鉴别的是( )
A. H2SO4 NaCl Na2CO3 CaCl2 B. HCl NaOH CuSO4 MgSO4
C. Na2CO3 K2SO4 BaCl2 HCl D. NaNO3 HCl CaCl2 KOH
难度: 困难查看答案及解析
-
除去食盐水中的CaCl2和Na2SO4杂质的操作有:①加过量的BaCl2溶液;②过滤;③加过量的Na2CO3溶液;④蒸发结晶;⑤加适量盐酸。下列操作顺序正确的是(提示BaSO4、BaCO3难溶于水)
A. ③①②⑤④ B. ①⑤③②④ C. ①③⑤④② D. ①③②⑤④
难度: 中等查看答案及解析
-
根据事物的某些相似性进行推理,并预测类似的可能性,是化学学习的一种重要思维方法,以下类推结果与实际不相符合的是( )
A.溶液具有均一性和稳定性,具有均一性和稳定性的液体一定是溶液
B.盐酸能使紫色石蕊试液变红色,能使紫色石蕊试液变红色的物质一定呈酸性
C.氢氧化钠溶液中有OH﹣,能与酸反应,氢氧化钾溶液中也有OH﹣,也能与酸反应
D.收集比空气轻的气体可用向下排空气法,能用向下排空气法收集的气体一定比空气轻
难度: 中等查看答案及解析
-
对实验过程的评价,正确的是( )
A. 向某无色溶液中滴入石蕊试液,石蕊试液变蓝色,则该溶液是碱溶液
B. 某溶液滴加BaCl2试液,生成不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO42﹣
C. 某溶液滴加稀HCl,无现象,再滴加BaCl2试液生成白色沉淀,则该溶液含有SO42﹣
D. 某钠盐溶液加入稀盐酸后会产生CO2气体,则该溶液是Na2CO3溶液
难度: 中等查看答案及解析
-
下列生活、生产或化学实验行为必须涉及到化学变化的是( )
(1)配制食盐溶液选种
(2)除铁锈
(3)氢氧化钠变质
(4)海水制镁
(5)海水淡化
(6)海水晒盐
(7)除去粗盐中不溶性杂质
(8)除去粗盐中可溶性杂质
(9)海水制碱
A. (2)(3)(4)(8)(9) B. (3)(4)(8)(9)
C. (2)(3)(7)(8)(9) D. (3)(4)(6)
难度: 简单查看答案及解析
-
下列选项中物质的俗名、化学式、类别、用途完全对应的是( )
A. 纯碱 Na2CO3碱制玻璃
B. 生石灰 CaO氧化物补钙剂
C. 食盐 NaCl盐除铁锈
D. 火碱 NaOH碱生产橡胶
难度: 中等查看答案及解析
-
能反映相关实验过程中量的变化的图象是( )
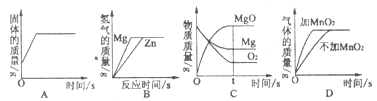
A. 用一氧化碳还原氧化铁
B. 等质量镁、锌分别和足量等质量分数的盐酸反应
C. 镁在氧气中燃烧
D. 等质量、等质量分数的双氧水完全分解
难度: 困难查看答案及解析
-
下列离子能在pH=2的水溶液中大量共存的是( )
A. SO42﹣、NO3﹣、K+、OH﹣ B. HCO3﹣、Cl﹣、SO42﹣、Na+
C. Cl﹣、NO3﹣、K+、Na+ D. NH4+、Cl﹣、OH﹣、K+
难度: 中等查看答案及解析
-
下列实验操作不能达到实验目的的是( )
选项
实验目的
实验操作
A
鉴别NaOH和NaCl固体
分别加少量水溶解
B
鉴别棉线和羊毛线
点燃后闻气味
C
除去H2中少量的水蒸气
将混合气体通过装有浓硫酸的洗气瓶
D
检验Na2CO3溶液中是否混有NaCl
加入过量的稀盐酸后,在滴加硝酸银溶液
难度: 中等查看答案及解析
-
甲乙两工厂的生产污水中各含有下列五种离子中的三种(两厂含有一种相同的离子):H+、Cu2+、K+、NO3、OH。若两厂单独排放都会造成严重的污染;若将两厂的污水按一定比例混合,沉淀后污水会变成只含有一种溶质的无色澄清溶液,此溶液可做化肥。下列关于污水的分析,正确的是
A.OH–和Cu2+来自同一工厂 B.Cu2+和K+来自同一工厂
C.K+和OH–来自同一工厂 D.H+和K+来自同一工厂
难度: 中等查看答案及解析
-
某学生设计的下列四个实验方案中,理论上正确,操作上可行,经济上合理的是( )
A. Cu
CuCl2
Cu(OH)2
B. H2O
O2
MgO
C. CaCO3
CaO
Ca(OH)2溶液
NaOH溶液
D. MgCl2
 Mg(OH)2
Mg(OH)2Mg
难度: 中等查看答案及解析
-
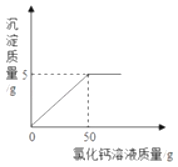
往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实验实施绘制如图所示曲线,下列说法正确的是( )
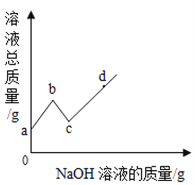
A.a至b段有蓝色沉淀生成
B.d点溶质种类为三种
C.c至d段,溶液pH不断减少
D.c点所含的溶质种类最少
难度: 困难查看答案及解析
-
已知在一定条件下发生反应:甲+乙→丙+丁,下列判断正确的是( )
A. 甲、乙、丙、丁不可能含有同一种元素
B. 丙为盐、丁为水,则该反应一定为复分解反应
C. 甲、乙为化合物,则该反应一定为复分解反应
D. 丙为Cu(NO3)2,则甲可能为单质、氧化物、碱或盐
难度: 中等查看答案及解析
-
如图所示,其中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质能发生反应,已知乙是铁.下列说法错误的是

A.五种物质中,只有铁是单质 B.丙是盐酸
C.戊是氢氧化钙 D.甲与丁反应属于复分解反应
难度: 困难查看答案及解析
-
某固体可能含有Ca(NO3)2、Na2SO4、Na2CO3、FeCl3、KCl中的一种或几种,现对其进行如下实验:①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液②取少量上述溶液,加过量稀硫酸,有气泡产生③取②所得溶液少量,滴加BaCl2溶液,产生白色沉淀.分析以上实验现象,对原固体组成的推断正确的是( )
A. 肯定有Na2CO3、Na2SO4,无FeCl3、Ca(NO3)2
B. 肯定有Na2CO3,无FeCl3、Ca(NO3)2
C. 肯定有Na2CO3、Na2SO4,无FeCl3
D. 肯定有Na2CO3,无FeCl3、KCl
难度: 中等查看答案及解析
-
在硝酸银、硝酸铜的混合溶液中加入一定量锌粉,反应停止后过滤,滤液仍为蓝色。有关判断正确的是( )
A. 滤渣中一定有银,没有铜和锌
B. 滤渣中一定有银和锌,可能有铜
C. 滤液中一定有硝酸锌、硝酸铜、硝酸银
D. 滤液中一定有硝酸锌、硝酸铜,可能有硝酸银
难度: 困难查看答案及解析
-
20℃时,将等质量的a、b两种固体,分别加入到盛有lO0g水的烧杯中,充分搅拌后现象如图甲,升温到50℃时,现象如图乙,a、b两种固体的溶解度曲线如图丙。下列说法正确的是
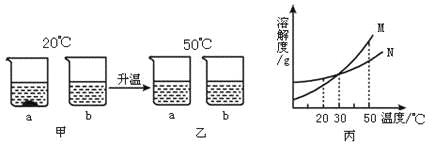
A. 图丙中M表示b的溶解度曲线
B. 图甲溶液中溶质的质量分数a大于b
C. 图乙中a、b溶液一定是不饱和溶液
D. 30℃时a、b溶液溶质质量分数不相等
难度: 困难查看答案及解析
-
在已经调平的托盘天平两边各放一只等质量的烧杯,向烧杯中各加入质量相同、质量分数相等的稀硫酸,然后在左右两盘的烧杯中分别放入等质量的锌粉和铁粉。下列实验现象不可能观察到的是
A. 天平指针开始偏向放铁粉的烧杯一边
B. 只有铁粉有剩余
C. 天平指针最终偏向放锌粉的烧杯一边
D. 只有锌粉有剩余
难度: 中等查看答案及解析
-
向四个烧杯中各加入质量相等、质量分数相等的稀硫酸,然后各加入镁、氧化镁、氢氧化镁、碳酸镁都恰好完全反应。则四个烧杯中溶质质量分数最小的是加入( )
A. 镁 B. 氧化镁 C. 氢氧化镁 D. 碳酸镁
难度: 中等查看答案及解析