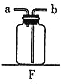-
俗话说:“五谷杂粮壮身体,青菜萝卜保平安”,其中“萝卜青菜”富含的营养素是( )
A. 糖类 B. 脂肪 C. 蛋白质 D. 维生素
难度: 简单查看答案及解析
-
加油站内必须张贴的图标是
A.
 B.
B.  C.
C.  D.
D. 
难度: 简单查看答案及解析
-
下列物质的用途中,利用其化学性质的是( )
A. 氧气用于气焊 B. 浓硫酸用作干燥剂
C. 铜用于制导线 D. 用活性炭除去冰箱异味
难度: 简单查看答案及解析
-
下列物质由分子构成的是( )
A. 水 B. 铝 C. 金刚石 D. 氯化钠
难度: 简单查看答案及解析
-
下列净水方法中,净化程度最高的是( )
A. 吸附 B. 沉淀 C. 过滤 D. 蒸馏
难度: 简单查看答案及解析
-
环境保护是我国的一项基本国策。下列行为有利于环境保护的是
A. 焚烧废弃塑料 B. 深埋处理废旧电池
C. 控制企业排污 D. 丢弃实验剩余药品
难度: 简单查看答案及解析
-
下列物质的化学式和俗名对应不相符的是
A. Hg-水银 B. NaHCO3-苏打 C. NaOH-苛性钠 D. C2H5OH-酒精
难度: 简单查看答案及解析
-
溶液与我们的日常生活密切相关。下列关于溶液的说法正确的是( )
A. 溶液一定是无色透明的 B. 面粉与水混合可形成溶液
C. 稀溶液也可能是饱和溶液 D. 溶液的上层浓度小,下层浓度大
难度: 简单查看答案及解析
-
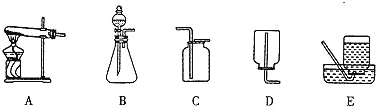
下列操作正确的是( )
A. 滴加液体
B. 塞进橡胶塞
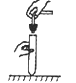 C. 测量溶液pH
C. 测量溶液pH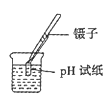 D. 检查装置气密性
D. 检查装置气密性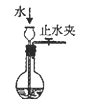
难度: 简单查看答案及解析
-
下列区分物质的方法错误的是( )
A. 用燃着的木条区分氮气和二氧化碳
B. 用氯化钡溶液区分稀盐酸和稀硫酸
C. 用水区分硝酸铵固体和氢氧化钠固体
D. 用点燃闻气味的方法区分羊毛纤维和合成纤维
难度: 简单查看答案及解析
-
生活中处处充满化学。下列说法正确的是( )
A. 食用加碘盐可以预防人体贫血
B. 用细沙灭火降低了可燃物着火点
C. 洗洁精清除油污利用了乳化作用
D. 施用大量的化肥农药以提供农作物的产量
难度: 简单查看答案及解析
-
下列事实的结论或解释错误的是( )
A. 分离液态空气制氧气——说明分子可以再分
B. 桂花开放时满园飘香——说明分子在不断运动
C. 气体可压缩储存于钢瓶中——说明分子之间有间隔
D. 酸碱中和反应都能生成水——实质是H+与OH—结合生产了H2O
难度: 简单查看答案及解析
-
下列各组物质中,能相互反应且反应后溶液总质量增加的是( )
A. 铁和硫酸铜溶液 B. 氧化铁固体和稀硫酸
C. 盐酸和澄清石灰水 D. 氯化钠溶液和硝酸钾溶液
难度: 简单查看答案及解析
-
下列实验方案合理的是( )
选项
实验目的
所用试剂或方法
A
实验室制取二氧化碳
块状大理石与稀硫酸
B
鉴别硬水和软水
观察液体是否浑浊
C
鉴别水、氯化钾溶液
硝酸银溶液
D
除去二氧化碳中少量的一氧化碳
通入氧气,点燃
A. A B. B C. C D. D
难度: 简单查看答案及解析