-
下列各组离子在pH=1的溶液中能大量共存,并形成无色透明溶液的是( )
A. Fe3+、NO3﹣、OH﹣ B. K+、NO3﹣、CO32﹣
C. Ba2+、MnO4﹣、SO42﹣ D. NH4+、Cl﹣、SO42﹣
难度: 困难查看答案及解析
-
逻辑推理是化学学习中常用的思维方法。下列说法正确的是
A. 化合物含有不同种元素,则由不同种元素组成的纯净物一定是化合物
B. 常温下,碱溶液的 pH 大于 7,碳酸钠溶液的 pH 也大于 7,则碳酸钠属于碱
C. 置换反应中一定有元素化合价发生变化,则有元素化合价发生变化的反应一定是置换反应
D. 酸能使紫色石蕊试液变红,通入二氧化碳后的紫色石蕊试液变红,则二氧化碳属于酸
难度: 中等查看答案及解析
-
下列有关物质的化学式、名称、俗名不完全对应的是( )
A. NaCl氯化钠食盐 B. CaO氧化钙熟石灰
C. Na2CO3碳酸钠纯碱 D. NaOH氢氧化钠烧碱
难度: 中等查看答案及解析
-
物质存放在烧杯中一段时间后,质量变大且变质的是( )
①浓盐酸②浓硫酸③烧碱④生石灰⑤碱石灰
A. ③④⑤ B. ②③④⑤ C. ①②③④⑤ D. ④⑤
难度: 中等查看答案及解析
-
下列化肥中,从外观即可与其他化肥相区别的是
A. 磷矿粉 B. 硝酸铵 C. 硫酸钾 D. 氯化钾
难度: 简单查看答案及解析
-
在Ca(OH)2的饱和溶液中加入下列物质,冷却至室温,溶液的pH没有改变的是( )
A.CO2 B.CaO C.Cu(NO3)2 D.HCl
难度: 中等查看答案及解析
-
下列物质间的转化,不能一步完成的是( )
A.Fe→Cu B.KNO3→NaNO3 C.Mg→MgO D.H2SO4→HCl
难度: 中等查看答案及解析
-
公园里部分植物的枝叶枯黄,茎也比较纤细。建议工作人员最好给这些植物施用的一种化肥是( )
A. NH4HCO3 B. KNO3 C. Ca(H2PO4)2 D. (NH4)3PO4
难度: 中等查看答案及解析
-
下列各组常见的固体物质中,用水不能区分的是( )
A.NaOH和NH4NO3
B.CuSO4和Na2SO4
C.Na2CO3和CaCO3
D.NaCl和KCl
难度: 困难查看答案及解析
-
用pH试纸测溶液的pH,是今年我市化学实验操作考查的题目之一,下列有关pH试纸的使用说法正确的是( )
A. 把pH试纸浸入待测液 B. 用湿润的玻璃棒蘸取待测液
C. 把显色的pH试纸与标准比色卡对照读数 D. 测出石灰水的pH为12.4
难度: 中等查看答案及解析
-
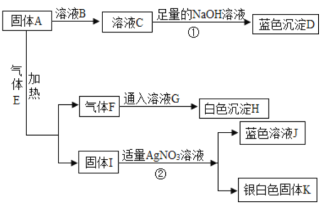
下图物质经-步反应转化的两种途径,相关说法正确的是

A. 氧化物为SO2
B. X只能是硫酸
C. ②可能有沉淀生成
D. ①②属于复分解反应
难度: 中等查看答案及解析
-
向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是
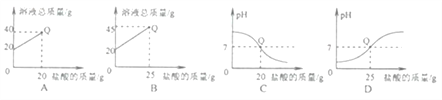
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
由Mg、MgO、Mg(OH)2、MgCO3组成的混合物,共20.6g加入182g16%的盐酸后,恰好完全反应后可得到 198.5g 溶液,所得溶液中溶质的质量分数为( )
A. 18.7% B. 19.1% C. 20.8% D. 38%
难度: 困难查看答案及解析