-
现有三组溶液:①汽油和氯化钠溶液 ②39%的乙醇溶液 ③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是
A. 分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D. 蒸馏、萃取、分液
难度: 简单查看答案及解析
-
下列仪器中,可直接用酒精灯加热的是( )
①烧杯;②坩埚;③锥形瓶;④蒸发皿;⑤试管;⑥圆底烧瓶;⑦容量瓶
A. ②④⑤ B. ①②⑤⑥ C. ②④⑥⑦ D. ①②③⑤
难度: 中等查看答案及解析
-
下图所示是分离混合物时常用的主要仪器,从左至右,可以进行的混合物分离操作分
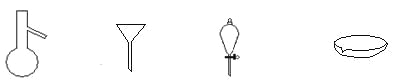
A. 蒸馏、蒸发、萃取、过滤 B. 蒸馏、过滤、萃取、蒸发
C. 萃取、过滤、蒸馏、蒸发 D. 过滤、蒸发、萃取、蒸馏
难度: 简单查看答案及解析
-
用某种仪器量取液体体积时,平视时读数为x mL,仰视时读数为y mL,俯视时读数为z mL,若y<x<z,则所用仪器可能是( )
A. 酸式滴定管 B. 碱式滴定管 C. 量筒 D. 以上仪器都不是
难度: 中等查看答案及解析
-
下列分离物质的方法中,根据沸点不同进行分离的是( )
A. 蒸馏 B. 萃取 C. 重结晶 D. 蒸发
难度: 简单查看答案及解析
-
不能用来萃取碘水中的碘的物质是( )
A. 汽油 B. 苯 C. 酒精 D. 四氯化碳
难度: 中等查看答案及解析
-
下列有关说法正确的是( )
A. 物质的量不是国际单位制中的基本物理量
B. 某物质含有4 mol氧
C. 阿伏加德罗常数就是6.02×1023 mol-1
D. 常用“物质的量”表示一定数目微观粒子的集合体
难度: 中等查看答案及解析
-
有下列三种含杂质的气体(括号内为杂质):
①CO2(HCl); ②H2(HCl); ③NH3(水蒸气)。某学生欲除去以上气体中的杂质依次选用了三种试剂,该学生选用的试剂均正确的是( )
A. NaHCO3溶液、NaOH溶液、碱石灰
B. Na2CO3溶液、浓硫酸、碱石灰
C. NaHCO3溶液、NaOH溶液、浓硫酸
D. NaOH溶液、浓硫酸,碱石灰
难度: 中等查看答案及解析
-
从海带中提取碘的实验过程中涉及下列操作,其中正确的是( )
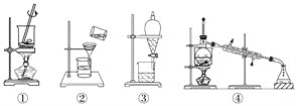
A. ①将海带灼烧成灰 B. ②过滤得含I-的溶液
C. ③放出碘的苯溶液 D. ④分离碘并回收苯
难度: 简单查看答案及解析
-
下列实验操作中,错误的是
A. 蒸发操作时,不能使混合物中的水分完全蒸干后,才停止加热
B. 蒸馏操作时,应使温度计水银球与蒸馏烧瓶的支管口处相平
C. 分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大
难度: 中等查看答案及解析
-
与OH - 具有相同质子数和电子数的粒子是( )
A. H2O B. F C. Na+ D. NH2-
难度: 中等查看答案及解析
-
在0.5 mol Na2SO4中,含有Na+ 数约是( )
A. 6.02×1023 B. 3.01×1023 C. 0.5 D. 1
难度: 简单查看答案及解析
-
设NA为阿伏加德罗常数的数值,下列叙述错误的是( )
A. 标准状况下,11.2 L氦气中含有0.5NA个原子
B. 2.4g镁完全反应生成镁离子,失去的电子数目一定为0.1NA
C. 常温常压下,46 g NO2和N2O4的混合气体中含有原子总数为3NA
D. 1 mol Na完全反应生成钠离子,失去的电子总数为NA
难度: 中等查看答案及解析
-
a mol O2气体和a mol O3气体相比较,下列叙述一定正确的是
A. 体积相等 B. 分子数相等 C. 原子数相等 D. 质量相等
难度: 简单查看答案及解析
-
设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A. 常温常压下,100 g 98%硫酸溶液中含有的氧原子数为4NA
B. 标准状况下,1 mol H2、N2混合气体的体积约为22.4 L
C. 15 g CH3+中含有的电子数为0.8NA
D. 1 mol H2O2分子中含有1 mol H2,1 molO2
难度: 中等查看答案及解析
-
在标准状况下,若VL甲烷中含有的氢原子个数为b,则阿伏加德罗常数可表示为 ( )
A. Vb/22.4 B. 22.4b/V C. Vb/5.6 D. 5.6b/V
难度: 中等查看答案及解析
-
只给出表中甲和乙对应的量,不能用来求物质的量的是( )
甲
乙
A
物质的微粒数
阿伏加德罗常数
B
标准状况下气体摩尔体积
标准状况下气体体积
C
固体体积
固体密度
D
非标准状况下物质的质量
物质的摩尔质量
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
如果a g某气体中含有的分子数为b,则c g该气体在标准状况下的体积是(式中NA为阿伏加德罗常数的值)( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 25℃,1.01×105 Pa, 64g SO2中含有的原子数为3NA
C. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
D. 标准状况下,11.2LH2O 含有的分子数为0.5NA
难度: 中等查看答案及解析
-
在标准状况下,与32 g O2的体积相等的N2的( )
A. 质量为14 g B. 体积为22.4 L
C. 分子数为6.02×1024 D. 物质的量为2 mol
难度: 中等查看答案及解析
-
下列叙述中正确的是 ( )
①在标准状况下,0.2 mol任何物质的体积均为4.48 L
②当1 mol气体的体积为22.4 L时,它一定处于标准状况下
③标准状况下,1 L HC1和1 L H2O的物质的量相同
④标准状况下,lg H2和14 g N2的体积相同
⑤28 g CO的体积为22.4 L
⑥同温同压下,气体的密度与气体的相对分子质量成正比
A.①②③④ B.②③⑥ C.⑤⑥ D.④⑥
难度: 中等查看答案及解析
-
下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5mol NH3 ②标准状况下22.4L He ③7.2g H2O ④0.2mol H3PO4
A. ①④③② B. ④③②①
C. ②③④① D. ①④②③
难度: 中等查看答案及解析
-
标准状况下,4.48g某气体的分子数与2.8 g CO分子数相等,则该气体的密度为 ( )
A. A . 2.0g·L-1 B. B . 20.0 g·L-1 C. C . 0.2 g·L-1 D. D . 0.4g·L-1
难度: 中等查看答案及解析
-
由CO2、CO组成的混合气体在同温同压下与氧气的密度相同,则该混合气体中CO2与CO的体积比可为( )
A. 3∶2 B. 1∶4 C. 1∶3 D. 3∶1
难度: 中等查看答案及解析