-
2017年暑期,科普纪录片《我们需要化学》风靡朋友圈。下列提法与该主题一致的
A. 水什么时候都能灭火
B. 本化妆品纯天然,不含任何化学物质
C. 服用钙片可以预防感冒
D. 化学是人类进步的阶梯
难度: 简单查看答案及解析
-
生活中有很多物质分离提纯或转化的实例,跟实验室用到的方法原理相同或相近。下列描述的过程与分离方法不匹配的是
A. 用乙醚提取青蒿素--萃取
B. 海水晒盐--蒸发
C. 活性炭脱色--过滤
D. 从石油中分离出煤油、柴油--蒸馏(含分馏)
难度: 简单查看答案及解析
-
油罐车上所贴的危险化学品标志是
A. 易燃液体 B. 剧毒品 C. 氧化剂 D. 遇湿易燃物品
难度: 简单查看答案及解析
-
下列有关摩尔质量的说法,正确的是
A. CO2的摩尔质量等于它的相对分子质量
B. H2的摩尔质量,等于6.02×1023个氢气分子的质量
C. H2O的摩尔质量为18g
D. Al(OH)3与Na2O2的摩尔质量相同
难度: 简单查看答案及解析
-
实验室提纯含少量氯化钠杂质的硝酸钾的过程如下图所示。下列分析正确的是
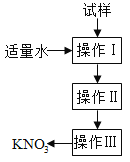
A. 操作Ⅰ是过滤,将固体分离除去
B. 操作Ⅱ是加热浓缩。趁热过滤,除去杂质氯化钠
C. 操作Ⅲ是过滤、洗涤,将硝酸钾晶体从溶液中分离出来
D. 操作Ⅰ~Ⅲ总共需两次过滤
难度: 中等查看答案及解析
-
如图表示1g O2与1g气体X在相同容积的密闭容器中压强(p)与温度(T)的关系,则气体X可能是( )
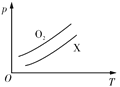
A. C2H4 B. CH4 C. NO D. CO2
难度: 困难查看答案及解析
-
欲除去某溶液里混有的少量杂质,下列做法中不正确的是(括号内的物质为杂质)
A. NaCl溶液(BaCl2):加过量Na2CO3溶液,过滤,再加适量盐酸并加热
B. KNO3溶液(AgNO3):加过量KCl溶液,过滤
C. NaCl溶液(Br2):加CCl4,萃取分液
D. 碘单质I2(NaCl):加热升华后,再凝华
难度: 中等查看答案及解析
-
下列各组物质中,所含分子数相同的是( )
A.10gH2和10gO2 B.5.6LN2和11gCO2
C.9gH2O和0.5molBr2 D.224mLH2(标准状况)和0.1molN2
难度: 中等查看答案及解析
-
密闭容器中充有氢气、氧气和氯气,用电火花点燃后均恰好完全反应,产物经冷却得溶质质量分数为33.3%的盐酸,则原容器中三种气体的体积比为
A. 3∶1∶1 B. 4∶1∶2 C. 8∶4∶1 D. 9∶4∶1
难度: 困难查看答案及解析