-
医院在进行外科手术时,常用HgCl2稀溶液作为手术刀的消毒剂,已知HgCl2有如下性质:①HgCl2晶体熔点较低 ②HgCl2熔融状态下不导电 ③HgCl2在水溶液中可发生微弱电离。下列关于HgCl2的叙述中正确的是( )
A. HgCl2晶体属于分子晶体
B. HgCl2属于离子化合物
C. HgCl2属于电解质,且属于强电解质
D. HgCl2属于非电解质
难度: 中等查看答案及解析
-
化学与生活、社会发展息息相关。下列有关说法正确的是
A. 二氧化硫可广泛用于食品的增白
B. “青蒿一握,以水二升渍,绞取汁”,青蒿素的提取属于化学变化
C. 碳酸钡可用于胃肠X射线造影检查
D. 绿色化学要求从源头上消除或减少生产活动对环境的污染
难度: 中等查看答案及解析
-
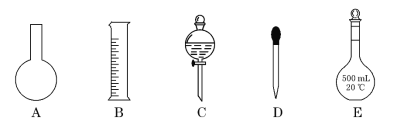
下列各种仪器: ①漏斗 ②容量瓶 ③滴定管 ④分液漏斗 ⑤天平 ⑥量筒 ⑦胶头滴管 ⑧蒸馏烧瓶。常用于物质分离的是( )
A. ①③⑦ B. ②⑥⑦ C. ①④⑧ D. ④⑥⑧
难度: 中等查看答案及解析
-
下列有关实验操作的叙述错误的是
A. 过滤操作中,漏斗的尖端应接触烧杯内壁
B. 从滴瓶中取用试剂时,滴管的尖嘴可以接触试管内壁
C. 滴定接近终点时,滴定管的尖嘴可以接触锥形瓶内壁
D. 向容量瓶转移液体时,导流用玻璃棒可以接触容量瓶内壁
难度: 中等查看答案及解析
-
NA为阿伏伽德罗常数的值,下列叙述正确的是( )
A. 1.0L1.0mo1·L-1的NaAlO2水溶液中含有的氧原子数为2NA
B. 120g二氧化硅中含有硅氧键的个数为4NA
C. 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1 NA
D. 28g乙烯和环丙烷中含有4NA个氢原子
难度: 简单查看答案及解析
-
在配制一定物质的量浓度的盐酸时,下列错误操作可使所配制溶液的浓度偏高的是
A. 用量筒量取浓盐酸时俯视量筒刻度进行读数
B. 溶解搅拌时有液体飞溅
C. 定容时俯视容量瓶瓶颈刻度线
D. 摇匀后见液面下降,再加水至刻度线
难度: 简单查看答案及解析
-
下列反应的离子方程式正确的是 ( )
A. 用醋酸除去水垢:2H++CaCO3===Ca2++CO2↑+H2O
B. 酸性氯化亚铁溶液中加入双氧水2Fe2++H2O2===2Fe3++O2↑+2H+
C. NaAlO2溶液中通入过量CO2:2AlO2—+CO2+3H2O=2Al(OH)3↓+CO32-
D. 电解饱和食盐水获取烧碱和氯气:2Cl-+2H2O
H2↑+Cl2↑+2OH-
难度: 中等查看答案及解析
-
实验是化学研究的基础,下列关于各实验装置的叙述正确的是( )
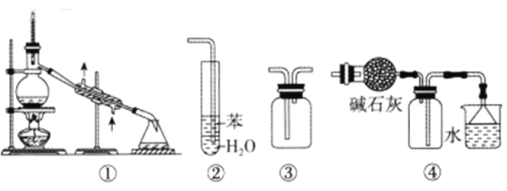
A. 装置③可用于收集H2、CO2、Cl2、NH3等气体
B. 装置②可用于吸收NH3或HCl气体,并防止倒吸
C. 装置①常用于分离互不相溶的液体混合物
D. 装置④可用于干燥、收集氯化氢,并吸收多余的氯化氢
难度: 简单查看答案及解析
-
我国明代《本草纲目》中收载药物1892种,其中“烧酒”条目下写道:“自元时始创其法,用浓酒和糟入甑,蒸令气上……其清如水,味极浓烈,盖酒露也。”这里所用的“法”是指( )
A. 萃取 B. 渗析 C. 蒸馏 D. 干馏
难度: 简单查看答案及解析
-
在三个密闭容器中分别充入CO、CH4、O2三种气体,当它们的温度和密度都相同时,这三种气体的压强(p)从大到小的顺序是( )
A. p(CO)>p(CH4)>p(O2) B. p(O2)>p(CO)>p(CH4)
C. p(CH4)>p(O2)>p(CO) D. p(CH4)>p(CO)>p(O2)
难度: 简单查看答案及解析
-
下列叙述正确的是(用NA代表阿伏加德罗常数的值)( )
A. 2.4 g 金属镁变为镁离子时失去的电子数为0.1NA
B. 1 mol HCl气体中的粒子数与0.5 mol·L-1盐酸中溶质的粒子数相等
C. 在标准状况下,22.4 L CH4与18 g H2O所含有的电子数均为 10NA
D. CO和N2为等电子体,22.4 L CO气体与1 mol N2所含的电子数相等
难度: 中等查看答案及解析
-
下列说法正确的是
A. 0.012 kg 12C中含有约6.02×1023个碳原子
B. 1 mol H2O中含有2 mol氢和1 mol氧
C. 氢氧化钠的摩尔质量是40 g
D. 0.1 mol氢气和2.24 L氯化氢气体所含分子数相同
难度: 简单查看答案及解析
-
在同温同压下,相同体积的甲、乙两种气体的质量比是17∶14。若乙气体是CO,则甲气体可能是( )
A. H2S B. HCl C. NH3 D. Cl2
难度: 中等查看答案及解析
-
在一定条件下,某化合物X受热分【解析】
2XA↑+2B↑+4C↑,测得反应后生成的混合气体对H2的相对密度为11.43,在相同条件下,X的相对分子质量是( )
A. 11.43 B. 22.85 C. 80.01 D. 160.02
难度: 简单查看答案及解析
-
NA表示阿伏加德罗常数,下列叙述正确的是( )
A. 等物质的量的N2和CO所含分子数均为NA
B. 一定温度下,1 L 0.5 mol·L-1 NH4Cl溶液与2 L 0.25 mol·L-1 NH4Cl溶液含NH4的物质的量相同
C. 1 mol Na2O2固体中含离子总数为3NA
D. 标准状况下,2.24 L 苯所含分子数为0.1NA
难度: 简单查看答案及解析
-
下列数量的各物质所含原子个数按由大到小顺序排列的是( )
①0.5 mol 氨气 ②4 g 氦气 ③4 ℃时9 mL水 ④0.2 mol H3PO4
A. ①④③② B. ④③②① C. ②③④① D. ①④②③
难度: 简单查看答案及解析
-
设NA为阿佛加德罗常数的值,下列叙述正确的是( )
A. 0.1L 0.5mol/L CH3COOH溶液中含有的氢离子数为0.05NA
B. 0.2 mol NaHSO4晶体中含有的阳离子数为0.4NA
C. 22.4 L(标准状况)氩气含有的质子数为18NA
D. 标准状况下,4.48 L CCl4含有的共价键数为0.8NA
难度: 中等查看答案及解析
-
分类是学习和研究化学的一种常用的科学方法。下列分类合理的是
①根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
②根据反应中是否有电子转移将化学反应分为氧化还原反应和非氧化还原反应
③根据氧化物的组成将氧化物分为酸性氧化物、碱性氧化物和两性氧化物
④根据反应的热效应将化学反应分为放热反应和吸热反应
⑤根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
A. 只有②④ B. 只有②③④ C. 只有①②④ D. 只有②③④⑤
难度: 简单查看答案及解析
-
阿伏加德罗常数约为NA。下列叙述中正确的是 ( )
A. I L 0.1mol/L的FeCl3溶液中,H+的数目约为0.1NA
B. 1 mol金刚石中含有C-C键的数目为2NA
C. 7.8 g Na2O2中含有的阴离子数目约为0.2NA
D. 标准状况下,l L甲醇完全燃烧后生成的CO2分子个数约为(1/22.4)NA
难度: 简单查看答案及解析
-
下列各组物质各自形成晶体,均属于分子晶体的化合物是( )
A. NH3、HD、C2H4 B. PCl3、CO2、SiO2
C. H2SO4、SO3、NH3 D. CCl4、Na2S、H2O2
难度: 简单查看答案及解析
-
下列各组物质都是化合物的是( )
A. 氨气、溴蒸气、氯气 B. 汽油、甘油、煤焦油
C. 冰、干冰、冰醋酸 D. 王水、重水、石灰水
难度: 简单查看答案及解析
-
下列各组离子中,可能能大量共存的是( )
A. 加入铝粉有氢气产生的溶液中:Na+、CO32-、C1-、K+
B. pH = 14的无色溶液中:Na+、K+、HCO3-、NO3-
C. 在0.1mol/L的盐酸溶液中:Fe2+、Na+、ClO-、Ca2+
D. 在c(H+)/c(OH-)= 1×10-12 的溶液中:NH4+、Ca2+、C1-、K+
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. 氯气跟水反应:Cl2+H2O=2H++Cl-+ClO-
B. 硫酸铜溶液跟氢氧化钡溶液反应:Ba2++SO42-=BaSO4↓
C. 碳酸钠溶液中加入少量稀盐酸:CO32- + H+ = HCO3-
D. 铜与稀盐酸反应:Cu + 2H+ = Cu2+ +H2↑
难度: 简单查看答案及解析
-
下列离子方程式书写正确的是
A. Mg(HCO3)2溶液与过量NaOH:Mg2++2HCO3-+2OH-=MgCO3↓+2H2O
B. 碳酸钙加入醋酸:CO32- + 2CH3COOH = CO2↑+ 2CH3COO- + H2O
C. 硫化亚铁跟盐酸反应:S2- + 2H+ = H2S↑
D. NaHSO4中加入Ba(OH)2至溶液呈中性:Ba2++2OH--+SO42- + 2H+=BaSO4↓+2H2O
难度: 简单查看答案及解析