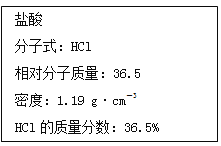
-
实验室中需要2 mol·L-1的NaCl溶液950 mL,配制时应选用的容量瓶的规格和称取的NaCl质量分别是
A. 950 mL,111.2 g B. 500 mL,117 g
C. 1 000 mL,117 g D. 任意规格,111.2 g
难度: 中等查看答案及解析
-
下列对实验过程的评价正确的是( )
A. 某固体中加入稀盐酸,产生了无色气体,证明该固体一定是CaCO3
B. 某溶液中滴加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,该溶液中一定含SO42—
C. 某无色溶液滴入无色酚酞试液显红色,该溶液一定显碱性
D. 验证烧碱溶液中是否含有Cl-,先加稀盐酸除去OH-,再加硝酸银溶液,有白色沉淀出现,证明含Cl-
难度: 简单查看答案及解析
-
某溶液中仅含有Na+、Mg2+、SO42-、Cl-四种离子(不考虑水电离出的H+和OH-),物质的量浓度之比为c(Na+)∶c(Mg2+)∶c(Cl-)=3∶5∶5。若Na+的物质的量浓度为3 mol·L-1,则SO42-的物质的量浓度为
A. 2 mol·L-1 B. 3 mol·L-1 C. 4 mol·L-1 D. 8 mol·L-1
难度: 简单查看答案及解析
-
在盛有碘水的试管中,加入少量CCl4后振荡,静置片刻后
A. 整个溶液变紫色 B. 整个溶液变为棕黄色
C. 上层为无色,下层为紫红色 D. 下层无色,上层紫红色
难度: 中等查看答案及解析
-
下列对“摩尔(mol)”的叙述不正确的是( )
A. 摩尔是一个单位,用于计量物质所含微观粒子的多少
B. 摩尔既能用来计量纯净物,又能用来计量混合物
C. 可以说“1 mol H2”但不能说“1 mol氢”
D. 摩尔是物质的微粒个数
难度: 简单查看答案及解析
-
若1 g CO2中含有x个原子,则阿伏加德罗常数可表示为
A. 1/44 mol-1 B. x/22 mol-1 C. 3x/44 mol-1 D. 44x/3 mol-1
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
C. 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
难度: 中等查看答案及解析
-
相同状况下,下列气体所占体积最大的是( )
A. 80g SO3 B. 16g O2 C. 32g H2S D. 3g H2
难度: 中等查看答案及解析
-
同温同压下,等质量的N2O4和NO2两种气体相比较,下列叙述正确的是( )
A. 体积比为2∶1 B. 分子个数之比为1∶1
C. 原子个数之比为1∶1 D. 氮原子个数之比为2∶1
难度: 中等查看答案及解析
-
如图两瓶体积相等的气体,在同温同压时瓶内气体的关系一定正确的是
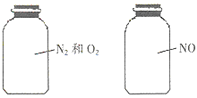
A. 所含原子数相等 B. 气体密度相等
C. 气体质量相等 D. 摩尔质量相等
难度: 中等查看答案及解析
-
在一定温度和压强下,1体积X2气和3体积Y2气化合生成2体积的一种气态化合物,则该化合物的化学式为( )
A. XY3 B. XY C. X3Y D. X2Y3
难度: 中等查看答案及解析
-
某种氢气和CO的混合气体,其密度是氧气的一半,则氢气的体积百分含量约为( )
A. 40% B. 46% C. 50% D. 54%
难度: 简单查看答案及解析
-
由CH4和O2组成的混合气体,标准状况下的密度为1g.L-1,则该混合气体中CH4和O2的体积比为( )
A. 2:1 B. 1:2 C. 2:3 D. 3:2
难度: 中等查看答案及解析
-
下列叙述正确的是( )
A. 含1 mol溶质的任何溶液,物质的量浓度一定相等
B. 配制1 mol·L-1 NaCl溶液1 L,其方法是将58.5 g NaCl溶于1 L水中即可
C. 体积相同、物质的量浓度相同的同种溶液所含溶质的微粒数一定相同
D. 1 L 0.5 mol·L-1 CaCl2溶液中,Ca2+和Cl-的物质的量浓度都是0.5 mol·L-1
难度: 简单查看答案及解析
-
下列溶液中与50 mL 1 mol·L-1的AlCl3溶液中氯离子浓度相等的是
A. 150 mL 1 mol·L-1 的NaCl B. 75 mL 2 mol·L-1 的NH4Cl
C. 150 mL 3 mol·L-1 的KCl D. 75 mL 2 mol·L-1 的CaCl2
难度: 简单查看答案及解析
-
某10%的 NaOH溶液,加热蒸发掉100g水后(无晶体析出)得到80mL 20%的NaOH溶液,则该20%的 NaOH溶液的溶质的物质的量浓度为( )
A. 6.25mol·L-1 B. 12.5mol·L-1 C. 7mol·L-1 D. 7.5mol·L-1
难度: 简单查看答案及解析
-
50 mL物质的量浓度为4.4 mol·L-1,密度为1.24 g·mL-1的稀硫酸的质量分数为( )
A. 35% B. 70% C. 17.5% D. 0.035%
难度: 简单查看答案及解析
-
下列溶液中,溶质的物质的量浓度不是1 mol·L-1的是( )
A. 10g NaOH固体溶解在水中配成250mL溶液
B. 将80g SO3溶于水并配成1L的溶液
C. 将0.5mol·L-1的NaNO3溶液100mL加热蒸发掉50g水的溶液
D. 标况下,将22.4L氯化氢气体溶于水配成1L溶液
难度: 简单查看答案及解析