-
日常生活中的下列做法,可用物质的化学性质解释的是( )
①用汽油洗掉衣服上的油污
②用纯碱除去面团因发酵产生的酸味
③用木炭除去冰箱内的异味 ④家庭中熬骨汤时,加入少量食醋可以增加汤中的钙质.
A.①②
B.②④
C.①③
D.②③④难度: 中等查看答案及解析
-
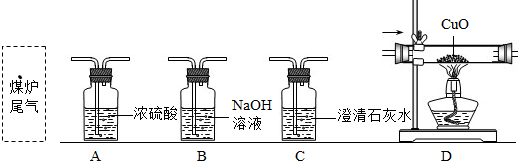
SO2是大气中的主要污染物,宜宾市SO2是大气的主要污染物,其中电厂是排放大户,因此,有专家认为,加大电厂SO2排污费征收力度,以促进绿色电厂建设,针对这一问题,某同学提出了以下控制SO2等有害气体排放的建议和措施:①提高排污收费标准 ②开发新能源,减少煤和石油的燃烧 ③通过洗煤将煤中10%~40%的可溶性硫酸除去 ④用NaOH和Na2CO3等碱性废液吸收烟气中的SO2.你认为可行的是( )
A.②③
B.①②③
C.③④
D.①②③④难度: 中等查看答案及解析
-
某化学课外活动小组在准备实验时配制了Na2SO4、Na2CO3、BaCl2、HCl四种溶液,因没及时贴标签,将其混淆.为将它们区别开来.把四种溶液编号为①②③④,进行了下面的实验:
按①②③④的顺序,由以上实验现象可以确定它们依次是( )实验内容 ①+② ②+④ ①+③ 实验现象 白色沉淀生成 白色沉淀生成 有气泡冒出
A.HCl、Na2SO4、Na2CO3、BaCl2
B.BaCl2、Na2CO3、Na2SO4、HCl
C.Na2CO3、BaCl2、HCl、Na2SO4
D.Na2SO4、BaCl2、Na2CO3、HCl难度: 中等查看答案及解析
-
某同学为探究Zn、Fe、Cu三种金属的活动性,设计了三组实验:
①将大小相同的Zn、Fe、Cu三种金属片分别插入体积和浓度均相同的稀硫酸中
②将Zn片插入硫酸铜溶液中,Cu片插入硫酸亚铁溶液中
③将Zn片插入硫酸亚铁溶液中,将Fe片插入硫酸铜溶液中
其中可以达到目的是( )
A.①③
B.③
C.①②
D.②③难度: 中等查看答案及解析
-
济宁玉堂酱有近300年的历史,产品有“味压江南”的美誉.我们家庭食用的玉堂陈醋是由高粱、大麦、豌豆等为主要原料经发酵制得的,醋酸的含量约在3.5%左右.下面关于醋酸的说法中,不正确的是( )
A.玉堂陈醋是混合物,它的主要成分是醋酸
B.醋酸是一种有机物,化学式为CH3COOH
C.醋酸是由碳、氢、氧三种元素组成的化合物,其元素个数比为1:2:1
D.每个醋酸分子中含有2个碳原子、4个氢原子和2个氧原子难度: 中等查看答案及解析
-
漂白粉的主要成分是氯化钙(CaCl2)和次氯酸钙[Ca(ClO)2],因其良好的消毒、漂白和除臭性能在日常生活中得到广泛应用,下面关于漂白粉的说法中,合理的是( )
A.氯化钙(CaCl2)和次氯酸钙[Ca(ClO)2]中氯元素的化合价相同
B.氯化钙(CaCl2)和次氯酸钙[Ca(ClO)2]都是无氧酸盐
C.氯化钙(CaCl2)属于盐类,次氯酸钙[Ca(ClO)2]属于氧化物
D.次氯酸钙[Ca(ClO)2]中含有原子团ClO难度: 中等查看答案及解析
-
解决下列问题所设计的实验方案中,合理可行的是( )
A.可根据气体燃烧的火焰来鉴别H2、CH4、CO三种气体
B.在空气中利用加热的方法除去氧化铜中的少量炭粉
C.区别氢氧化钠和碳酸钠溶液最简单的方法是滴加石蕊试剂手观察溶液颜色的变化
D.滴加氯化钡有白色沉淀生成,证明某溶液中一定含有CO32-或SO42-难度: 中等查看答案及解析
-
许多同学喜欢吃家庭腌制的小菜,腌制小菜的一般方法是:将食盐、香料等一起放入水中煮制得浓盐水,盐水冷却后放入洗净待腌制的鲜菜,腌制过程中还要不断打开缸盖晒缸并及时补充食盐,一段时间后,即得成品小菜,若室温时食盐的溶解度为36g,关于小菜腌制过程中的下列说法,错误的是( )
A.煮制浓盐水时,10kg水最多可得到浓盐水13.6kg
B.腌菜的过程中,原来的浓盐水会逐渐变稀
C.晒缸的目的一是防止腌菜腐败变质,二是促使水分蒸发以保持盐水的浓度
D.补充食盐的目的是保持盐水的浓度,以利用食盐往蔬菜中渗透难度: 中等查看答案及解析
-
根据不同化学反应的特点进行归纳、分类是我们学习、记忆化学反应的重要方法.分析下面化学反应,其中属于同一基本反应类型的是( )
①2H2O22H2O+O2↑
②CuO+H2Cu+H2O
③Fe3O4+4CO3Fe+4CO2
④2KI+Cl2=2KCl+I2
⑤Na2CO3+CO2+H2O=2NaHCO3
⑥BaCl2+H2SO4=BaSO4↓+2HCl.
A.①③⑤
B.②③④
C.②④
D.⑤⑥难度: 中等查看答案及解析
-
有一混合物是由盐酸、碳酸钠、硝酸钾、硫酸和氯化铜中的两种溶液混合而成.向该混合溶液中滴加氢氧化钡溶液,溶液体积的变化与生成沉淀质量的关系如右图所示,那么,这两种溶液是
( )
A.盐酸、硫酸
B.碳酸钠、硝酸钾
C.硝酸钾、盐酸
D.盐酸、氯化铜难度: 中等查看答案及解析