-
按照物质的组成和性质进行分类,HNO3应属于( )
①酸 ②氧化物 ③无氧酸 ④有氧酸 ⑤化合物 ⑥混合物 ⑦纯净物 ⑧一元酸
A. ①④⑤⑦⑧ B. ②③④⑤ C. ③④⑤⑦ D. ②⑤⑥⑦⑧
难度: 简单查看答案及解析
-
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取NaCl的质量分别是 ( )
A. 950mL,111.2g B. 500mL,117g C. 1000mL,117g D. 1000mL,111.2g
难度: 简单查看答案及解析
-
下雪时,常用融雪剂清理路面,醋酸钾(CH3COOK)是效果较好的融雪剂。下列关于1mol CH3COOK的叙述正确的是( )
A. 1mol CH3COOK含有1mol钾元素 B. CH3COOK的摩尔质量为98g
C. 1mol CH3COOK含有2mol氧 D. 1mol CH3COOK约含有3×6.02×1023个H
难度: 中等查看答案及解析
-
在0.5molNa2SO4中含有Na+的数目是( )个
A. 3.01×1023 B. 6.02×1023 C. 0.5 D. 1
难度: 简单查看答案及解析
-
关于“摩尔”叙述正确的是
A.摩尔是国际科学界建议采用的一种物理量
B.摩尔可以把物质的宏观数量与微观粒子的数量联系起来
C.摩尔是物质的量的单位,简称摩,符号为mol
D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩尔
难度: 中等查看答案及解析
-
下列关于阿伏加德罗常数的说法不正确的是 ( )
A. 6.02×1023就是阿伏加德罗常数
B. 0.012 kg 12C含有的碳原子数就是阿伏加德罗常数
C. 含有阿伏加德罗常数个粒子的物质的量是1 mol
D. 1 mol NH3所含原子数约是2.408×1024
难度: 简单查看答案及解析
-
NA表示阿伏加德罗常数的值,下列说法不正确的是( )
A. 64 g氧气中含氧分子数为2NA
B. 1.7 g OH-中所含的电子数为NA
C. 49 g硫酸中所含氧原子数为2NA
D. 58.5 g氯化钠中所含的离子数为NA
难度: 中等查看答案及解析
-
下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
A. 在常温常压下,11.2 L N2含有的原子数为NA
B. 32 g O2在标准状况下所占体积约为22.4 L
C. 标准状况下,18 g H2O所占的体积约为22.4 L
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
难度: 中等查看答案及解析
-
同温同压下,两种气体的体积如果不相同,请你推测其主要原因是( )
A. 气体的分子大小不同
B. 气体的物质的量不同
C. 气体分子的化学性质不同
D. 气体分子间的平均距离不同
难度: 中等查看答案及解析
-
关于同温、同压下等体积的N2O(气体)和CO2的叙述:①质量相同;②所含碳原子数与氮原子数相等;③所含分子数相等,其中正确的是( )
A. ①②③ B. ②③ C. ①② D. ①③
难度: 简单查看答案及解析
-
下列溶液中物质的量浓度为1 mol·L-1的是( )
A. 将40 g NaOH固体溶解于1 L水中
B. 将22.4 L氯化氢气体溶于水,配成1 L溶液
C. 将1 L 10 mol·L-1的浓盐酸与9 L水混合
D. 10 g NaOH固体溶解在水中,配制成250 mL溶液
难度: 简单查看答案及解析
-
从2 L 1 mol·L-1 NaOH溶液中取出100 mL,下列有关这100 mL溶液的叙述不正确的是 ( )
A. 浓度为0.1 mol·L-1 B. 浓度为1 mol·L-1 C. 含NaOH 4 g D. 含NaOH 0.1 mol
难度: 简单查看答案及解析
-
用固体样品配制一定物质的量浓度的溶液,需经过称量、溶解、转移溶液、定容等操作。下列图示对应的操作规范的是( )
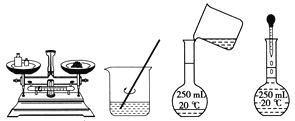
A. 称量 B. 溶解 C. 转移 D. 定容
难度: 简单查看答案及解析
-
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl-的物质的量浓度之比为 ( )
A. 1∶1∶1 B. 1∶2∶3 C. 3∶2∶1 D. 3∶4∶3
难度: 中等查看答案及解析
-
已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
A. 16g B. 32g C. 64g /mol D. 32g /mol
难度: 简单查看答案及解析
-
关于容量瓶的四种叙述:①是配制准确浓度溶液的仪器;②不宜贮存溶液;③不能用来加热;④使用之前要检查是否漏水。这些叙述中正确的是()
A. ①②③④ B. ②③ C. ①②④ D. ②③④
难度: 中等查看答案及解析
-
出现大雾天气时,致使高速公路关闭,航班停飞,雾属于下列分散系中的 ( )
A. 溶液 B. 悬浊液 C. 乳浊液 D. 胶体
难度: 简单查看答案及解析
-
晚自习的课间,同学们站在四楼上,可以看到市里的空中有移动的光柱,这就是气溶胶发生的丁达尔效应,下列说法不正确的是 ( )
A. 胶体和溶液都是混合物,它们属于不同的分散系
B. 胶体分散质粒子的直径介于1~100 nm之间
C. 利用丁达尔效应可鉴别胶体和溶液
D. 胶体经短时间静置后会产生沉淀
难度: 简单查看答案及解析
-
用饱和的氯化铁溶液制取氢氧化铁胶体,正确的操作是( )
A. 将饱和氯化铁溶液滴入氢氧化钠溶液中即可
B. 将饱和氯化铁溶液滴入热水中,生成棕黄色液体即可
C. 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色液体即可
D. 将饱和氯化铁溶液滴入沸水中,并继续煮沸至生成红褐色沉淀即可
难度: 简单查看答案及解析
-
以下表示的是碳及其化合物的相互转化关系:C
CO2→H2CO3→CaCO3→CO2其中涉及的基本反应类型依次为( )
A. 置换、化合、分解、复分解
B. 置换、化合、复分解、分解
C. 化合、置换、分解、复分解
D. 化合、置换、复分解、分解
难度: 简单查看答案及解析
-
适度饮水有益于健康,但过量饮水使体内电解质浓度过低,导致生理紊乱而引起“水中毒”,下列属于人体内常见电解质的是 ( )
A. CO2 B. NaCl C. BaSO4 D. 葡萄糖
难度: 简单查看答案及解析
-
下列电离方程式书写正确的是
A.NaOH=Na++O2-+H+
B.FeCl3=Fe3++Cl3-
C.Ca(NO3)2=Ca2++2(NO3)2-
D.H2SO4=2H++SO42-
难度: 简单查看答案及解析