-
设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 常温常压下,8.8 g CO2和N2O混合气体中所含的电子数为4.4 NA
B. 6.72 L NO2与水充分反应转移的电子数目为0.2 NA
C. 1.0 L 1.0 mol/L的NaAlO2水溶液中含有的氧原子数为2 NA
D. 64 g加热了的铜丝在硫磺蒸气里完全反应后,失去的电子数为2 NA
难度: 中等查看答案及解析
-
化学与工农业生产、生活密切相关,下列说法中正确的是
A. 合成纤维和光导纤维都是新型有机非金属材料
B. 淀粉、纤维素和油脂都属于天然高分子化合物
C. “玉不琢不成器”、“百炼方能成钢”发生的均为化学变化
D. 造纸工艺中使用明矾,会导致纸张发生酸性腐蚀,使纸张变脆,易破损。
难度: 简单查看答案及解析
-
下列叙述中正确的是
A. 由乙酸和乙醇生成乙酸乙酯的反应类型和由乙醇生成乙烯的反应类型相同
B. 丙烯在一定条件下可与氯气发生取代反应生成3-氯丙烯
C. 硫酸铵和硝酸铅均能使蛋白质变性
D. 甲苯与氯气在光照下发生取代反应主要生成2,4-二氯甲苯
难度: 简单查看答案及解析
-
短周期元素A、B、C、D、E在元素周期表中的相对位置如图所示,其中D原子的质子数是其M层电子数的三倍,下列说法不正确的是 ( )
A. A有5种正价,与B可形成6种化合物
B. 工业上常通过电解熔融态C2B3的方法来获得C的单质
C. 简单离子的半径由大到小为:E>A>B>C
D. D、E两元素形成的化合物每种原子最外层都达到了8e-稳定结构
难度: 中等查看答案及解析
-
锂空气电池充放电基本原理如图所示,下列说法不正确的是
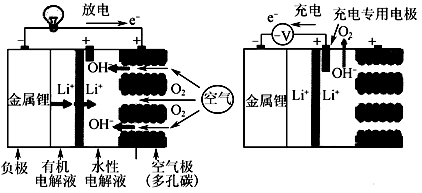
A. 充电时,锂离子向阴极移动
B. 充电时阴极电极反应式为Li++e-===Li
C. 放电时正极电极反应式为O2+4e-+2H2O===4OH-
D. 负极区的有机电解液可以换成水性电解液
难度: 困难查看答案及解析
-
用式量是71的烃基取代乙苯苯环上的一个氢原子,能得到的有机物共有(不含立体异构)
A. 8种 B. 16种 C. 24种 D. 36种
难度: 中等查看答案及解析
-
下列有关说法中不正确的是
A. 某温度时的混合溶液中c(H+)=
mol·L-1,说明该溶液呈中性(KW为该温度时水的离子积常数)
B. 常温下,由水电离出的c(H+)=10-12mol·L-1的溶液的pH可能为2或12
C. 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO
且浓度均为0.010 mol·L-1溶液中逐滴加入0.010 mol·L-1的AgNO3溶液时,CrO
先产生沉淀
D. 常温下pH=7的CH3COOH和CH3COONa混合溶液中,c(Na+)=c(CH3COO-)
难度: 困难查看答案及解析


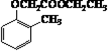 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下: