-
安全是生产、生活中的头等大事,安全大于一切,化学实验中的安全也不例外,也需引起我们的高度重视。那么在盛放浓硫酸的试剂瓶的标签上应印有下列警示标志中的( )

A. A B. B C. C D. D
难度: 简单查看答案及解析
-
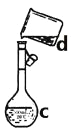
2015年10月5日,屠呦呦获2015年诺贝尔生理学奖或医学奖,成为首获科学类诺贝尔奖的中国人,也是第一位获得诺贝尔科学奖项的中国本土科学家。屠呦呦获奖的原因是她发现了青蒿素,青蒿素是从青蒿茎叶中提取出来的一种高效抗疟疾药。下列中草药煎制步骤中,属于过滤操作的是( )
A.
 冷水浸泡 B.
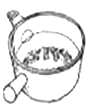
冷水浸泡 B. 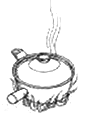 加热煎制 C.
加热煎制 C. 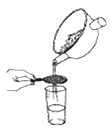 箅渣取液 D.
箅渣取液 D. 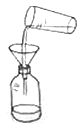 灌装保存
灌装保存难度: 简单查看答案及解析
-
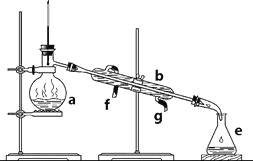
规范的操作是实验成功的保证。下列实验操作正确的是 ( )
A.
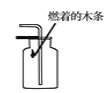 CO2的验满 B.
CO2的验满 B.  收集O2 C.
收集O2 C.  滴加液体 D.
滴加液体 D. 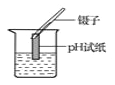 测溶液pH
测溶液pH难度: 中等查看答案及解析
-
在下列试剂中,能够鉴别BaCl2 、NaCl 、Na2CO3的最佳试剂是( )
A. 稀盐酸 B. NaOH溶液 C. 稀硫酸 D. AgNO3溶液
难度: 中等查看答案及解析
-
化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法不正确的是( )
A. 油条的制作口诀是“一碱、二矾、三钱盐”,其中的“碱”是烧碱
B. 黑火药的最优化配方是“一硫二硝三木炭”,其中的“硝”是硝酸钾
C. 过滤操作要领是 “一贴二低三靠”,其中“贴”是指滤纸紧贴漏斗的内壁
D. “固体需匙或纸槽,一送二竖三弹弹;块固还是镊子好,一横二放三慢竖”。前一个固体一般指粉末状固体
难度: 极难查看答案及解析
-
一氧化二氮(N2O)又称笑气,是无色有甜味的气体,在室温下稳定,有轻微麻醉作用,其麻醉作用于1799年由英国化学家汉弗莱·戴维发现,该气体早期被用于牙科手术的麻醉,现用在外科手术和牙科起麻醉和镇痛作用。现有agN2O含b个分子,用NA表示阿伏加德罗常数的数值,则NA可表示为( )
A. a/44b B. 28b/a C. 28a/b D. 44b/a
难度: 中等查看答案及解析
-
新华社哈尔滨9月14日电:记者从黑龙江省相关部门获悉,13日14时40分黑龙江省鸡东县裕晨煤矿发生瓦斯爆炸,有9名矿工遇难。研究表明瓦斯中甲烷(CH4)与氧气的质量比为1:4时极易爆炸,则此时瓦斯中甲烷与氧气的体积比为( )
A. 2:1 B. 1:2 C. 1:1 D. 1:4
难度: 中等查看答案及解析
-
传统的引爆炸药中含有铅(Pb),使用时会产生无染,同时其引爆后的剩余炸药还严重危害接触者的人身安全。美国UNC化学教授Thomas J·Meyer等研发了环境友好、安全型的“绿色”引爆炸药,其中一种可表示为Na2R,爆炸后不会产生危害性残留物。已知10ml的Na2R溶液中含Na+的微粒数为N个,该Na2R溶液的物质的量浓度为( )
A. N×10-2 mol·L-1 B. N/(1.204×1022) mol·L-1
C. N/(6.02×1021) mol·L-1 D. N/(6.02×1025) mol·L-1
难度: 中等查看答案及解析
-
在某温度下,NaOH的溶解度为20g,该温度下将80gNaOH放入220g水中,充分搅拌后,测得溶液的密度为1.2g·ml-1,则溶液中溶质的物质的量浓度为( )
A. 0.02mol·L-1 B. 2.0mol·L-1 C. 5.0mol·L-1 D. 7.5mol·L-1
难度: 中等查看答案及解析
-
标准状况下,有:①6.72L CH4 ②3.01×1023个HCl ③13.6g H2S ④0.2molNH3,对这四种气体的关系有以下四种表述:
a.体积:②>③>①>④ b.物质的量:②>③>④>① c.质量:②>③>①>④ d.氢原子个数:①>③>④>②其中正确的是( )
A. abc B. bcd C. abcd D. acd
难度: 中等查看答案及解析
-
下列溶液中Cl﹣浓度与150mL 1mol·L﹣1CaCl2溶液中Cl﹣浓度相等的是( )
A. 100mL 1 mol·L﹣1的FeCl3溶液 B. 75 mL 2 mol·L﹣1NH4Cl溶液
C. 100 mL 1.5mol·L﹣1的NaCl溶液 D. 150 mL 1 mol·L﹣1的KCl溶液
难度: 中等查看答案及解析