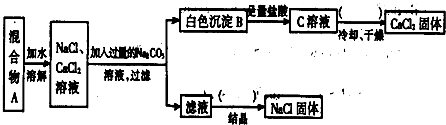
-
某溶液中Cl-、Br-、I-三者物质的量之比是1:2:3,通入一定量的Cl2,当反应完成后,该比值变为3:2:1,则反应的Cl2与原溶液中I-的物质的量之比是( )
A.1:2
B.1:4
C.1:3
D.1:6难度: 中等查看答案及解析
-
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700℃时制造出纳米级金刚石粉末.该成果发表在世界权威的《科学》杂志上,立刻被科学家们高度评价为“稻草变黄金”.同学们对此有下列一些理解,其中错误的是( )
A.金刚石属于金属单质
B.制造过程中元素种类没有改变
C.CCl4是一种化合物
D.这个反应是置换反应难度: 中等查看答案及解析
-
必须加入氧化剂后才能发生的变化是( )
A.Cl2→Cl-
B.Cl-→Cl2
C.Cu2+→Cu
D.CO32-→CO2难度: 中等查看答案及解析
-
下列溶液中的Cl-与50mL 1mol•L-1 AlCl3溶液中Cl-物质的量相等的是( )
A.150mL 1mol•L-1的NaCl溶液
B.75mL 2mol•L-1NH4Cl溶液
C.75mL 1mol•L-1的FeCl3溶液
D.150mL 2mol•L-1的KCl溶液难度: 中等查看答案及解析
-
下列物质中,能使淀粉碘化钾溶液变蓝的是( )
A.久制的氯水
B.碘水
C.KBr
D.KI难度: 中等查看答案及解析
-
放射性同位素53125I可用于治疗肿瘤.该同位素原子核内的中子数与核外的电子数之差是( )
A.72
B.19
C.53
D.125难度: 中等查看答案及解析
-
任何原子都具有的粒子是( )
A.质子和中子
B.中子和电子
C.质子、电子和原子核
D.中子、电子和原子核难度: 中等查看答案及解析
-
下列各组物质,在物质的分类中,前者从属于后者的一组是( )
A.金属、非金属
B.纯净物、混合物
C.氧化物、化合物
D.单质、化合物难度: 中等查看答案及解析
-
下列不属于分散系的是( )
A.CuSO4溶液
B.水
C.豆浆
D.CO2通入澄清石灰水后所得体系难度: 中等查看答案及解析
-
下列四种化学操作名称从左到右分别是( )
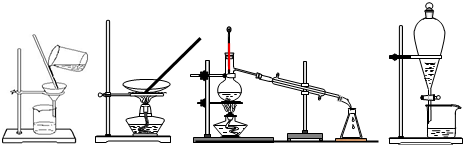
A.过滤、蒸发、蒸馏、分液
B.过滤、蒸馏、蒸发、分液
C.蒸发、蒸馏、过滤、分液
D.分液、蒸馏、蒸发、过滤难度: 中等查看答案及解析
-
原子X核内质子数等于中子数,其阳离子Xn+核外共有a个 电子,则X的质量数为( )
A.2(a+n)
B.2(a-n)
C.2a
D.n+2难度: 中等查看答案及解析
-
1mol水蒸气,18mL液态水(密度为1g/cm3),18g冰(密度为0.9g/cm3)中含的分子数是( )
A.水蒸气中最多
B.冰中最多
C.液态水中最多
D.一定相等难度: 中等查看答案及解析
-
为了证明氯酸钾晶体中含氯元素,选用给出的试剂和操作,其操作顺序正确的是:( )
①滴加AgNO3溶液 ②加水溶解 ③过滤、取滤液 ④与二氧化锰混合加热 ⑤加稀HNO3⑥与浓盐酸反应 ⑦与NaOH溶液加热 ⑧用淀粉碘化钾.
A.⑥⑦①⑤
B.⑥⑧
C.④②③①⑤
D.②①⑤难度: 中等查看答案及解析
-
7.1克氯气与下列金属完全反应时,消耗金属质量最多的是( )
A.铝
B.铁
C.镁
D.钠难度: 中等查看答案及解析
-
在①S2-、②Fe2+、③Fe3+、④Mg2+、⑤S、⑥I-、⑦H+ 中,只有氧化性的是( )
A.②③④⑤
B.③④⑦
C.①⑥
D.②⑤难度: 中等查看答案及解析
-
下列气体发生装置相同的是( )
A.氯气和氢气
B.氯气和氧气
C.氢气和二氧化碳
D.氧气和二氧化碳难度: 中等查看答案及解析
-
砹是原子序数最大的卤族元素,根据卤素性质的递变规律,对砹及其化合物的叙述不正确的是( )
A.KAt核间距大于KBr
B.砹在常温下为有色固体
C.NaAt熔点较高
D.砹易溶于水难溶于四氯化碳难度: 中等查看答案及解析
-
某盐酸的ρ=1.18g/cm3,HCl的质量分数为36.5%.取200mL该盐酸与过量铁屑充分反应,若反应后溶液体积变化忽略不计,则FeCl2物质的量浓度是( )
A.5.9mol/L
B.1.18mol/L
C.11.8mol/L
D.无法计算难度: 中等查看答案及解析
-
设阿伏加德罗常数的值为NA,则下列说法正确的是( )
A.常温常压下,11.2L甲烷(CH4)中含有的氢原子数等于2NA
B.18g的NH4+离子中含有的电子数为10NA
C.1molFe与足量Cl2充分反应电子转移数为2NA
D.8gHe所含的分子数为2NA难度: 中等查看答案及解析
-
检验氯化氢气体中是否混有Cl2,可采用的方法是( )
A.湿润的有色布条
B.用干燥的蓝色石蕊试纸
C.气体中通入硝酸银溶液中
D.湿润的淀粉碘化钾试纸难度: 中等查看答案及解析