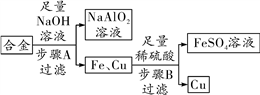
-
工业炼铁中会发生一氧化碳与氧化铁的反应,该反应中发生还原反应的物质是( )
A. CO B. Fe2O3 C. CO2 D. Fe
-
下列有关实验现象的描述中,正确的是
A. 加热试管内的碱式碳酸铜,绿色粉末逐渐变黑,试管口有小水滴
B. 细铁丝在氧气中燃烧,火星四射,生成红棕色固体
C. 镁条在空气中燃烧,产生黑烟,生成黑色粉末
D. 向少量氧化铜中加入稀硫酸,有气泡产生,黑色粉末逐渐消失,溶液变蓝
-
在试管中放入一根镁条(已去除氧化膜),往其中加入硝酸银溶液至浸没镁条,观察到如下现象:
①镁条表面迅速覆盖一层疏松的固体物质,经检验发现生成的固体物质中有单质银;
②镁条表面有明显的气泡现象,经检验发现气泡中有氢气;对于上述实验现象的分析错误的是
A. 镁能从硝酸银溶液中置换出银
B. 镁跟硝酸银溶液反应会生成氢气
C. 镁投入硝酸银溶液中只发生2AgNO3+Mg=Mg(NO3)2+2Ag
D. 根据该实验可判断镁比银化学活动性强
-
2017年5月5日,我国国产大型客机C919在上海浦东机场首飞成功,标志着我国航空事业有了重大突破。结合所学知识回答下列问题:
(1)大型客机大量使用了铝锂合金、钛合金等,其原因是合金比纯金属具有____。
(2)空气中,铝比铁具有更好的抗腐蚀性,原因是_________(用文字叙述)。
(3)已知金属M和N能够发生如下反应:Fe+MCl2=== M+FeCl2,N+FeCl2=== Fe+NCl2,判断Fe、M、N三种金属的活动性由强到弱的顺序是___。
-
金属R与AgNO3溶液发生反应:R+2AgNO3=== R(NO3)2+2Ag,下列说法正确的是( )
A. R可能是铝 B. 在金属活动顺序里,R一定排在氢前面
C. Ag的金属活动性比R强 D. 反应前后R的化合价发生了改变
-
下列物品所使用的主要材料为有机合成材料的是
A. 陶瓷花瓶 B. 纯棉帽子
B. 纯棉帽子
C. 黄金首饰 D. 塑料油瓶
D. 塑料油瓶
-
下列金属制品中,利用金属导电性的是
A. 铝箔 B. 铁锅 C. 铜导线 D. 金项链
-
下列属于铁的物理性质的是
A. 易生锈 B. 能导电 C. 能与稀硫酸反应 D. 能在氧气中燃烧
-
下列关于金属材料的说法中,不正确的是( )
A. 汞属于金属材料
B. 铜有良好的导电性,因而大量用于制作电线
C. 铝表面易生成致密氧化铝薄膜,因而具有良好的抗腐蚀性
D. 铝、铁、铜都是银白色金属
-
某电镀厂的电镀液中含有金盐,为了回收单质金,制作了如下图所示的“吸金球”,“吸金球”是将某种“吸金”物质装进纱袋,做成球状。将“吸金球”放入电镀液中,便会发生神奇的化学反应。综上所述,“吸金球”中的“吸金”物质可能是( )

A. 铁屑(Fe) B. 胆矾(CuSO4·5H2O)
C. 活性炭(C) D. 磁石(主要成分Fe3O4)
-
把一定质量的锌粉放入Cu(NO3)2溶液中,充分反应后过滤,向滤渣中加入稀盐酸,有气体产生。下列对于滤渣的说法正确是
A. 只有Cu B. 只有Zn
C. 一定有Zn和Cu D. 一定有Cu,可能有Zn
-
向一定质量的稀硫酸中加入锌粉至过量,下列图像合理的是( )

A. A B. B C. C D. D
-
下列金属活动性最强的是( )
A. Zn B. Al C. Ag D. Fe
-
能与无色硝酸银溶液反应,使溶液变为蓝色的金属是( )
A. 铝 B. 铁 C. 铜 D. 银
-
一般情况下,将两种活泼性不同的金属放在潮湿的环境中,活泼性强的金属首先被腐蚀。为了避免轮船的钢质外壳被腐蚀,通常在外壳上镶嵌的金属是( )
A. 锌板 B. 铜板 C. 银板 D. 铅板
-
金属M与AgNO3溶液反应的化学方程式为:M+2AgNO3=== M(NO3)2+2Ag。下列说法不正确的是( )
A. 反应后的溶液可能为蓝色 B. 金属M可能是铝
C. M的金属活动性比Ag强 D. 反应前后M的化合价改变
-
为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论。则X溶液是
A. 稀硫酸 B. 硝酸银溶液 C. 氯化铜溶液 D. 氯化镁溶液
-
2.3g铁和M的混合物与足量的盐酸反应,生成0.2g氢气,则M可能是
A. 镁 B. 铝 C. 碳 D. 钠
-
现有X、Y、Z三种金属,把它们分别放入稀硫酸中,只有Z溶解并产生氢气;把X、Y分别放入硝酸银溶液中,只有X表面有银析出。则X、Y、Z的金属活动性由强到弱的顺序为( )
A. Z>X>Y B. Y>X>Z C. X>Y>Z D. Z>Y>X
-
下列图像能正确反映对应变化关系的是( )
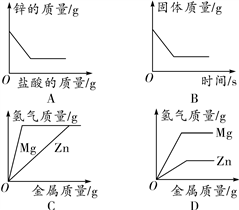
A. 向铜、锌混合物粉末中加入盐酸
B. 将铜片加入一定量的硝酸银溶液中
C. 向两份完全相同的稀盐酸中分别加入锌粉、镁粉
D. 向两份完全相同的稀盐酸中分别加入锌粉、镁粉
-
向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如右图所示。下列说法正确的是
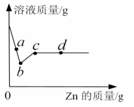
A. 取a点溶液,溶质为Zn(NO3)2和Cu(NO3)2
B. c点溶液中溶质为Zn(NO3)2
C. 若取b~c段固体,滴加稀盐酸,有气泡产生
D. 取d点的固体有2种
-
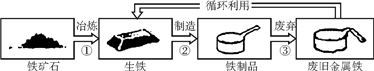
现有甲、乙、丙三种金属,采用将其中的一种金属分别放入另外两种金属的硫酸盐溶液中的方法进行实验,得到三种金属间的转化关系(如图所示)。则三种金属的活动性由弱到强的顺序是( )
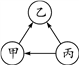
A. 甲 丙 乙 B. 丙 甲 乙 C. 乙 甲 丙 D. 甲 乙 丙
-
(题文)木炭还原氧化铜和一氧化碳还原氧化铜的实验装置如下图所示。
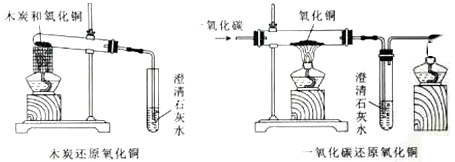
下列说法正确的是
A. 术炭、一氧化碳与氧化铜的反应都属于置换反应
B. 两个实验的相关反应中,只有碳元素的化合价发生改变
C. 两个实验中都可观察到红色固体变黑
D. 两个实验的操作中都要防止液体倒吸
-
现有一包由3.2g铜、13g锌和2g 碳组成的粉末,放到一定量的AgNO3溶液中,完全反应后得到的固体为m种,溶液中溶质为n种.下列说法中不正确的是( )
A. 若m=2,则n=2或3 B. 若固体中金属的质量为 48g,则m=4
C. 当m=3时,溶液可能呈蓝色 D. 反应后固体的质量不可能超过56g



 B. 纯棉帽子
B. 纯棉帽子
 D. 塑料油瓶
D. 塑料油瓶










 Mg
Mg