-
下列关于热化学反应的描述中正确的是
A.HCl和NaOH反应的中加热△H =-57.3 kJ/mol,则H2SO4和Ca(OH) 2反应的
中和热△H =2×(-57.3)kJ/mol
B.CO(g)的燃烧热是283.0 kJ/mol,则2CO2(g)
2CO(g)+O2(g)反应
的△H = +2×283.0 kJ/mol
C.需要加热才能发生的反应一定是吸热反应
D.1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
难度: 中等查看答案及解析
-
C+CO2
2CO △H 1>0,反应速率v1 ,N2+3H2
2NH3 △H 2<0,反应速率v2 。若升高温度,v1和v2的变化是
A.同时增大 B.同时减少 C.v1增大,v2减少 D.v1减少,v2增大
难度: 简单查看答案及解析
-
在一固定容积的密闭容器中,可逆反应: H2(g) + I2(g)
2HI (g)达到平衡的标志是
A.H2、I2、HI的分子数之比为1∶1∶2
B.混合气体的颜色不再发生变化
C.单位时间生成n mol H2,同时消耗成2n mol HI
D.混合气体的密度保持不变
难度: 中等查看答案及解析
-
下列叙述中,不能用平衡移动原理解释的是
A.红棕色的NO2,加压后颜色先变深后变浅
B.黄绿色的氯水光照后颜色变浅
C.由H2、Br2(g)、HBr(g)气体组成的平衡体系加压后颜色变深
D.工业合成氨反应中加压有利于提高氨气的产率
难度: 中等查看答案及解析
-
金属锡的冶炼常用焦炭作还原剂:SnO2(s)+2C(s)==Sn(s)+2CO(g)↑,反应过程中能量的变化如图所示。下列有关该反应的ΔH、ΔS的说法中正确的是
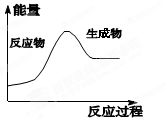
A.ΔH<0 ΔS<0 B.ΔH>0 ΔS<0
C.ΔH<0 ΔS>0 D.ΔH>0 ΔS>0
难度: 中等查看答案及解析
-
下列操作中,能使电离平衡H2O
H++OH-向右移动且溶液呈酸性的是
A.向水中加入NaHSO4溶液 B.向水中加入Al2(SO4)3固体
C.向水中加入Na2CO3溶液 D.将水加热到100℃,使pH=6
难度: 中等查看答案及解析
-
下列操作正确的是
A.用pH试纸测得某新制氯水的pH值为3.5
B.用标准盐酸溶液滴定一定体积的待测NaOH溶液时,用待测溶液润洗锥形瓶
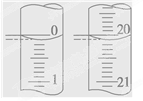
C.用酸式滴定管量取酸性高锰酸钾溶液5.10mL
D.用10mL的量筒量取8.05mL浓硫酸
难度: 中等查看答案及解析
-
一定量的盐酸跟过量的铁粉反应时,为了减缓反应速率,且不影响生成氢气的总量,可向盐酸中加入适量的
①NaOH固体 ②KNO3溶液 ③硫酸钾溶液 ④CH3COONa固体
A.①③ B.③④ C.②③ D.②④
难度: 中等查看答案及解析
-
下列反应中,属于水解反应且书写正确的是
A.CH3COOH+OH-
CH3COO-+H2O
B.HCO3—+ H2O
CO32- + H3O+
C.NH4+ + H2O
NH3·H2O + H+
D.S2- + H2O
H2S+ OH-
难度: 中等查看答案及解析
-
下列有关问题,与盐的水解有关的是
①NH4Cl与ZnCl2溶液可作焊接金属中的除锈剂
②明矾可作净水剂
③草木灰与铵态氮肥不能混合施用
④实验室盛放碳酸钠溶液的试剂瓶不能用磨口玻璃塞
⑤加热蒸干AlCl3溶液并灼烧得到Al2O3固体
A.①②③ B.②③④ C.①④⑤ D.①②③④⑤
难度: 中等查看答案及解析
-
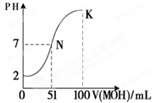
有等体积、等PH的Ba(OH)2、NaOH和NH3·H2O三种碱溶液,滴加等浓度的盐酸将它们恰好中和,用去酸的体积分别为V1、V2、V3,则三者的大小关系正确的是
A.V3>V2=V1 B.V3=V2=V1 C.V3>V2>V1 D.V1=V2>V3
难度: 中等查看答案及解析
-
为证明某可溶性一元酸(HX)是弱酸,有如下实验方案,其中不合理的是
A.室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸
B.室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸
C.相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸
D.将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸
难度: 中等查看答案及解析
-
可逆反应A(?)+aB(g)
C(g)+2D(g)(a为正整数)。反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
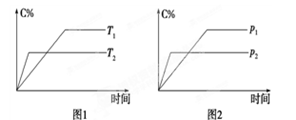
A.若a=2,则A为液态或固体
B.该反应的正反应为放热反应
C.T2>T1,P2>P1
D.其他条件不变,增加B的物质的量,平衡正向移动,平衡常数K增大
难度: 困难查看答案及解析
-
已知某温度下,几种酸的电离常数如下:Ka(HCN)= 6.2×10-10 mol/L、Ka(HF)= 6.8×10-4 mol/L、Ka(CH3COOH)= 1.8×10-5 mol/L、Ka(HNO2)= 6.4×10-6mol/L。则物质的量浓度都为0.1 mol/L的下列溶液中,pH最小的是
A.NaCN B.NaF C.CH3COONa D.NaNO2
难度: 中等查看答案及解析
-
已知醋酸达到电离平衡后,改变某条件电离平衡向正反应方向移动,则下列说法正确的是
A.实现该变化的只能是升高温度B.溶液的导电能力一定变强
C.溶液的pH一定减小D.发生电离的分子总数增多
难度: 中等查看答案及解析
-
在给定的四种溶液中,加入以下各种离子,各离子能在原溶液中大量共存的是
A.滴加石蕊试液显红色的溶液:Fe3+、NH4+、Cl-、I-
B.pH值为1的溶液:Cu2+、Na+、Mg2+、NO3-
C.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO3-、Br-、Ba2+
D.所含溶质为Na2SO4的溶液:K+、CO32-、NO3-、Al3+
难度: 中等查看答案及解析
-
物质的量浓度相同的下列溶液中, NH4+浓度最大的是
A.NH4Cl B. CH3COO NH4 C.NH4HSO4 D.NH4HCO3
难度: 中等查看答案及解析
-
已知298 K,101 kPa时,2SO2(g)+O2(g)
2SO3(g) ΔH=-197 kJ·mol-1。在相同温度和压强下,向密闭容器中通入2 mol SO2和1 mol O2,达到平衡时,放出热量为Q1,向另一个体积相同的容器中通入1 mol SO2,0.5 mol O2 和1 mol SO3,达到平衡时放出热量为Q2,则下列关系正确的是
A.Q2<Q1<197 kJ·mol-1 B.Q2=Q1=197 kJ·mol-1
C.Q1<Q2<197 kJ·mol-1 D.Q2=Q1<197 kJ·mol-1
难度: 中等查看答案及解析
-
下列叙述正确的是
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3•nH2O
A.①②③④⑤ B.①③④⑤ C.①③⑤ D.②④
难度: 中等查看答案及解析
-
常温下有体积相同的四种溶液:①pH=3的CH3COOH溶液 ②pH=3的盐酸 ③pH=11的氨水④pH=11的NaOH溶液。下列说法正确的是
A.若将四种溶液稀释100倍,溶液pH大小顺序:③>④>①>②
B.③和④分别用等浓度的硫酸溶液中和,消耗硫酸溶液的体积:③=④
C.①与②分别与足量镁粉反应,生成H2的量:①<②
D.②和③混合,所得混合溶液的pH大于7
难度: 中等查看答案及解析
-
下图为一原电池装置,下列叙述中正确的是
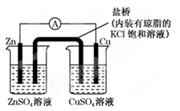
A.铜是阳极,铜片上有气泡产生
B.盐桥中的K+ 移向ZnSO4溶液
C.电流从锌片经导线流向铜片
D.铜离子在铜片表面被还原
难度: 中等查看答案及解析
-
常温下,下列溶液中的粒子浓度关系正确的是
A.新制氯水中加入固体NaOH:c(Na+)=c(Cl-)+c(ClO-)+c(OH-)
B.pH=8.3的NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3)
C.25℃时,浓度均为0.1 mol·L-1的CH3COOH、CH3COONa混合溶液pH=4.75,c(
)+c(
)=c(CH3COOH)+c(H+)
D.一定物质的量浓度的Na2S溶液中:c(OH-) =c(H+)+2c(H2S) + c(HS-)
难度: 困难查看答案及解析
-
某同学按图示装置进行实验:A极是铜锌合金,B极为纯铜,溶液为足量的硫酸铜溶液。通电一段时间后,若A极恰好全部溶解,此时B极质量增加5.76g,溶液质量增0.03g,则合金中Cu、Zn原子个数比为
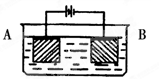
A.4:1 B.3:1 C.2:1 D.任意比
难度: 中等查看答案及解析
-
某温度下,已知Ksp(BaSO4 )= 1.1×10-10,Ksp(BaCO3)=2.5×10-9。下列说法正确的是
A.BaSO4比BaCO3溶解度小,所以,BaCO3 不可能转化为BaSO4
B.BaCO3 、BaSO4均不溶于水,所以都可以做钡餐试剂
C.任何温度下,向Na2CO3溶液中加入BaCl2和Na2SO4,当两种沉淀共存时,c(SO42—)/ c(CO32—) =4.4×10-2
D.该温度下,BaCO3若要在Na2SO4溶液中转化为BaSO4,则Na2SO4浓度至少为2.2×10-6 mol·L
难度: 中等查看答案及解析
-
利用如图装置,完成很多电化学实验。下列有关此装置的叙述中,正确的是
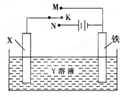
A. 若X为锌棒,Y为NaCl溶液,开关K置于M处,可减缓铁的腐蚀,这种方法称为牺牲 阴极保护法
B. 若X为碳棒,Y为NaCl溶液,开关K置于N处,可加快铁的腐蚀
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D.若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面镀铜,溶液中铜离子浓度将减小
难度: 中等查看答案及解析
-
盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
①Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ·mol-1
②3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=-47.4kJ·mol-1
③Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5kJ·mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:。
难度: 中等查看答案及解析
-
铅蓄电池的电池总反应式为:Pb+PbO2+4H++2SO42-
2PbSO4+2H2O
该电池放电时的正极反应式为________, 电池充电时的阴极反应式为。
难度: 中等查看答案及解析
-
有下图所示装置:
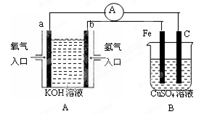
(1)装置A中b为 极,电极反应式为 ,a极反应式为 ;
(2)装置B中C为 极,电极反应式为 。
(3)当铁电极的质量变化为12.8g时,a极上消耗O2在标准状况下的体积为 L。
(4)若将装置B中的CuSO4溶液更换为100mL滴有酚酞的饱和NaCl溶液,电解一段时间后________极附近颜色变红,当装置A中消耗0.05mol氢气时,装置B中溶液的pH为________。
(5)若将装置B改为电解精炼铜,则粗铜作________极,另一极反应为________。
难度: 中等查看答案及解析