-
《本草衍义》中对精制砒霜过程有如下叙述,“取砒之法,将生砒就置火上,以器覆之,令砒烟上飞着覆器,遂凝结累然下垂如乳,尖长者为胜,平短者次之。”文中涉及的操作方法是
A. 蒸馏 B. 升华 C. 过滤 D. 萃取
难度: 中等查看答案及解析
-
下列化学操作中不正确的是
①配制溶液时,先向容量瓶中加入浓H2SO4,再加水稀释至刻度线
②向试管中滴加溶液时,为防止液体溅出,可将胶头滴管伸入试管内部
③闻未知气体气味时,可直接把集气瓶盖打开,放在鼻子下闻
④炮灭酒精灯时,应用扇子扇灭,而不能用嘴吹灭
A. 只有①②③ B. 只有①②④ C. 只有①③④ D. ①②③④
难度: 困难查看答案及解析
-
下列实验或实验操作达到实验目的的是
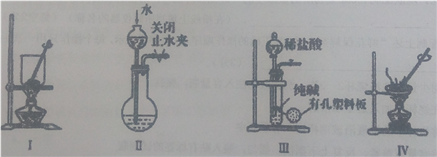
A. 图Ⅰ:将海带灼烧成灰
B. 图II:检验装置的气密性
C. 图Ⅲ:制取少量纯净的CO2气体
D. 图IV:蒸干NaHCO3饱和溶液制备NaHCO3晶体
难度: 简单查看答案及解析
-
正丁醛经催化加氢可制备1-丁醇。为提纯含少量正丁醛杂质的1-丁醇,现设计如下路线:

已知:①正丁醛与饱和NaHSO3溶液反应可生成沉淀;②乙醚的沸点是34℃,难溶于水,与1-丁醇互溶;③1-丁醇的沸点是118℃。则操作1~4分别是( )
A. 萃取、过滤、蒸馏、蒸馏 B. 过滤、分液、蒸馏、萃取
C. 过滤、蒸馏、过滤、蒸馏 D. 过滤、分液、过滤、蒸馏
难度: 中等查看答案及解析
-
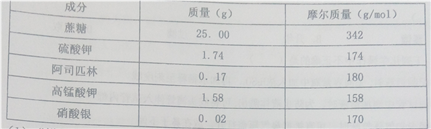
下列说法中,正确的是
A.
的摩尔质量是28g
B. 36 g H20中含有的原子总数约为6×6.02×1023
C. 0.5 mol O2的体积一定为11.2L
D. 1L 0.5 mol/L Na2CO3溶液中Na+的物质的量浓度为0.5mol/L
难度: 困难查看答案及解析
-
标准状况下,下列物质中体积最小的是
A. 0.lmo1CO2 B. 0.34g NH3 C. 18g H2O D. 1. 6g O2
难度: 简单查看答案及解析
-
阿伏加德罗常数的值为
,下列叙述中错误的是
①标准状况下,2. 24 L水中含有0.1
个水分子
②常温常压下,32g SO2含有的分子数约为3.01×1023
③2 mol NaOH的摩尔质量为80g/mol
④H2的气体摩尔体积约为22.4L/mol
⑤标准状况下,22.4L由N2和N2O组成的混合气体中,所含有的氮原子的物质的量为2mol
⑥2mol/L的CaCl2溶液中Cl-的数目为4
⑦常温常压下,lmol氧气含有的分子数为
⑧11.2 L氯气中含有氯原子数为NA
A. ①③④⑥⑧ B. ①④⑦⑧ C. ①④⑧ D. ②③④⑤⑦
难度: 中等查看答案及解析
-
同温同压下,a g甲气体和2a g乙气体所占的体积之比为1: 2,根据阿伏加德罗定律判断,下列叙述不正确的是
A. 同温同压下甲和乙的密度之比为1:1
B. 甲与乙的相对分子质量之比为1:1
C. 同温同体积下等质量的甲和乙的压强之比为1:1
D. 等质量的甲和乙中的原子数之比为1:1
难度: 中等查看答案及解析
-
某无色混合气体可能由CH4、H2、CO、CO2和HCl中的某几种气体组成。在恒温恒压条件下,通过过量的澄清石灰水未见变浑浊,但混合气体的总体积减小;把剩余气体导出后,在O2中能够点燃,燃烧产物不能使CuSO4粉末变色。则原混合气体的成份是
A HCl和CO B. HCl、H2和CO C.CH4和NH3 D. HCl、CO和CO2
难度: 中等查看答案及解析
-
现有一定量的气体如下:①标准状况下6.72L CH4 ②3.01×1023个HC1分子、③13.6gH2S、 ④0.2molNH3,这四种气体,从大到小排列中不正确的是
A. 标准状况下体积:②>③>①>④ B. 同温同压下的密度: ②>③>④>①
C. 氢原子个数:①>③>④>② D. 物质的量:①>③>④>②
难度: 中等查看答案及解析
-
如图所示,密闭筒形容器中,有活塞位于距全长一端1/5处,左边为空气,右边为H2、O2混合气体,标准状况下,若将H2、O2混合气体点燃引爆,活塞先左弹,恢复到原来温度后,活塞右滑停留在筒的中央,则原来H2、O2的物质的量比可能为 ( )
空气
H2、O2的混合气
A. 7:1 B. 1:1 C. 1:3 D. 4:1
难度: 极难查看答案及解析
-
在一定体积的密闭容器中放入20L气体P和37L气体W, 在一定条件下发生反应:3P(g)+4W(g) = 4R(g)+nY(g)反应完全后,容器温度不变,混合气体的压强是原来的92.5%,则化学方程式中的n值是
A. 3 B. 2 C. 5 D. 4
难度: 中等查看答案及解析
-
在V mL硫酸铝溶液中含m g铝离子,取该溶液V/3 mL用水稀释成2V mL,则稀释后的溶液中的硫酸根离子的物质的量浓度为
A. 250m/27V mol/L B. 125m/27V mol/L
C. 500m/27V mol/L D. 1000m/27V mol/L
难度: 困难查看答案及解析
-
甲、乙、丙是三种不含相同离子的可溶性物质。它们所含离子如下表所示:
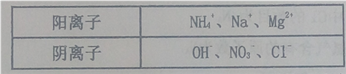
取等质量的三种化合物配制相同体积的溶液,其溶质物质的量浓度:c(甲)>c(乙)>c(丙),则乙物质可能是①MgCl2 ②NaOH ③NH4NO3
A. ① B. ② C. ③ D. ①②
难度: 中等查看答案及解析
-
质量分数为a%,物质的量浓度为cmol·L-1的NaCl溶液,蒸发溶剂,恢复到原来的温度,若物质的量浓度变为2cmol·L-1,则质量分数变为(蒸发过程中没有晶体析出)
A.等于2a% B.大于2a% C.小于2a% D.无法确定
难度: 困难查看答案及解析