-
C-NMR(核磁共振)可以用于含碳化合物的结构分析,有关
C的说法正确的是( )
A、质子数为6 B、电子数为13
C、中子数为6 D、质量数为6
难度: 简单查看答案及解析
-
铋(Bi)在医药方面有重要应用。下列关于
Bi和
Bi的说法正确的是( )
A.
Bi和
Bi都含有83个中子
B.
Bi和
Bi互为同位素
C.
Bi和
Bi的核外电子数不同
D.
Bi和
Bi分别含有126和127个质子
难度: 中等查看答案及解析
-
一定量的浓硝酸与过量的铜充分反应,生成的气体是( )
A.只有NO2 B.只有NO C.NO2和NO D.NO2和H2
难度: 中等查看答案及解析
-
下列各组中的离子,能在溶液中大量共存的是( )
A.H+ Na+ CO32- Cl- B.Ba2+ Na+ Cl- SO42-
C.K+ H+ SO42- OH- D.Ag+ Al3+ NO3- H+
难度: 中等查看答案及解析
-
已知X、Y均为1~18号之间的元素,X、Y可形成化合物X2Y和X2Y2,又知Y的原子序数小于X的原子序数,则两种元素的原子序数之和为( )
A.19 B.18 C.27 D.9
难度: 中等查看答案及解析
-
下列叙述正确的是 ( )
A.同周期元素中,VII A族元素的原子半径最大
B.现已发现的零族元素的单质在常温常压下都是气体
C.VI A族元素的原子,其半径越大,越容易得到电子
D.所有的主族元素的简单离子的化合价与其族序数相等
难度: 中等查看答案及解析
-
下列性质的递变中,正确的是
A、O、S、Na的原子半径依次增大
B、HF、NH3、SiH4的稳定性依次增强
C、LiOH、KOH、CsOH的碱性依次增强
D、HCl、HBr、HI的还原性依次减弱
难度: 中等查看答案及解析
-
元素R、X、T、Z、Q在元素周期表中的相对位置如下表所示, 其中R单质在暗处与H2剧烈化合并发生爆炸。则下列判断正确的是
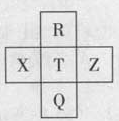
A.非金属性:Z<T<X
B.R与Q的电子数相差26
C.气态氢化物稳定性:R <T<Q
D.最高价氧化物的水化物的酸性:T>Q
难度: 中等查看答案及解析