-
邻羟基桂皮酸是合成香精的重要原料,下为合成邻羟基桂皮酸的路线之一
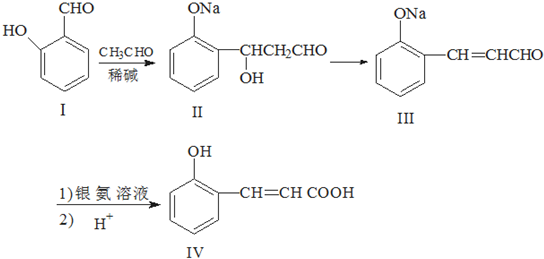
试回答下列问题:
(1)化合物II→化合物III的有机反应类型______
(2)化合物III在银氨溶液中发生反应化学方程式______
(3)有机物X为化合物IV的同分异构体,且知有机物X有如下特点:①是苯的对位取代物,②能与NaHCO3反应放出气体,③能发生银镜反应.请写出化合物X的结构简式______
(4)下列说法正确的是(双选)
A.化合物I遇氯化铁溶液呈紫色 B.化合物II能与NaHCO3溶液反应
C.1mol化合物IV完全燃烧消耗9.5molO2D.1mol化合物III能与3mol H2反应
(5)有机物R(C9H9ClO3)经过反应也可制得化合物IV,则R在NaOH醇溶液中反应的化学方程式为______.难度: 中等查看答案及解析
-
汽车排气中的CO、NOX已经成为大气的主要污染物,使用稀土等催化剂能将CO、NOx、碳氢化合物转化成无毒物质,从而减少汽车尾气污染.
(1)已知:N2(g)+O2(g)=2NO(g)△H=+180.5kJ/mol
2C(s)+O2(g)=2CO(g)△H=-221.0kJ/mol
C(s)+O2(g)=CO2(g)△H=-393.5kJ/mol
试写出NO与CO催化转化成N2和CO2的热化学方程式______
(2)在容积相同的两个密闭容器内(装有等量的某种催化剂),分别充入同量的NOx及C3H6,在不同温度下,同时发生以下反应:
18NO(g)+2C3H6(g)9N2(g)+6CO2(g)+6H2O(g);
18NO2(g)+4C3H6(g)9N2(g)+12CO2(g)+12H2O(g);
并分别在t秒时测定其中NOx转化率,绘得图象如右图所示:
①从图中可以得出的结论是
结论一:从测定NOX转化数据中判断,相同温度下______
结论二:______
②在上述NO2和C3H6反应中,提高NO2转化率的措施有______.(填编号)
A.加入催化剂 B.降低温度 C.分离出H2O(g) D.增大压强
(3)CO的中毒是由于CO与血液中血红蛋白的血红素部分反应生成碳氧血红蛋白,在37℃时:CO+Hb•O2O2+Hb•CO K=220
实验表明,Hb•CO的浓度即使只有Hb•O2浓度的2%,也可造成人的智力损伤.抽烟后,测得平衡时人体肺部的空气中CO和O2的浓度分别为10-6mol•L-1和10-2mol•L-1.请问,抽烟会造成人的智力损伤吗?(写出计算过程)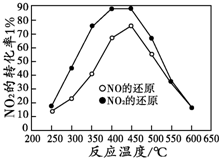
难度: 中等查看答案及解析
-
炼锌厂产生的工业废渣--锌渣(除了含Zn外,还含有Fe、Al、Cd和SiO2等杂质),利用锌渣制取并回收ZnSO4•7H2O和金属镉是一个有益的尝试,其流程如下:
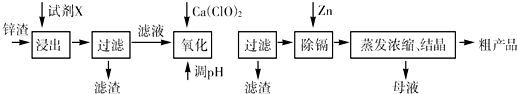
已知:Fe3+、Al3+、Zn2+、Cd2+、Fe2+以氢氧化物完全沉淀时的pH分别为:3.2,4.7,6.5,9.4,9.7
试回答下列问题:
(1)浸出时用到的试剂X为______
(2)写出加入Ca(ClO)2反应的离子方程式______
(3)调节pH过程可以选用______(填“ZnO”或“NaOH”);本流程的pH调节一般调至5,其目的是______
(4)写出过滤后加入过量的锌粉反应的离子方程式______
(5)在蒸发浓缩操作时,要采取实验措施______.难度: 中等查看答案及解析
-
化学兴趣小组的同学将Na2SO3在隔绝空气并经600℃以上的强热至恒重,然后对加热后固体进行元素定性定量分析,确定固体组成与Na2SO3无异;但把加热后固体溶于水,得到的溶液pH值比Na2SO3溶液的pH高.
(1)Na2SO3溶液呈______性(填“酸”或“碱”),其原理是(以相关的离子方程式表示)______.
(2)强热后的物质是什么呢?同学作如下探究
①分析猜想:Na2SO3在强热下发生了分解反应(自身氧化还原反应)
②该残留物可能的存在物质:
假设1:______;
假设2:______.
③设计实验方案证明你的假设,请按下表格式完成相关内容.实验步骤 预期现象和结论 步骤1:取少量固体分别于试管中,加入一定量的蒸馏水溶解 固体全部溶解 步骤2: 步骤3 难度: 中等查看答案及解析