-
下列化学药品与其危险化学品图形标志不一致的是
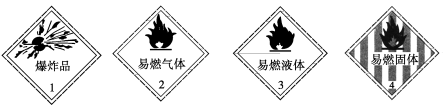
A.烧碱——1 B.甲烷——2 C.酒精——3 D.白磷——4
难度: 中等查看答案及解析
-
进行化学实验时必须注意安全,下列说法不正确的是
①不慎将酸溅到眼中,应立即用大量水冲洗,边洗边眨眼睛
②不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液
③不慎将浓盐酸洒在桌面上,应立即用浓氢氧化钠溶液冲洗
④配制稀硫酸时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸
⑤酒精洒到桌面上着火时可用水扑灭
A.①②③ B.②③④ C.③④⑤ D.全部
难度: 中等查看答案及解析
-
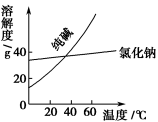
下列各组物质中,可按溶解、过滤、蒸发的操作顺序分离的是
A.氧化铜和炭粉 B.硝酸钾和氯化钠
C.水和酒精 D.碳酸钠和硫酸钡
难度: 中等查看答案及解析
-
下列制取蒸馏水的实验装置与操作的说法中,不正确的是
A.温度计的水银球应插入蒸馏烧瓶中的自来水中
B.冷凝管中的水流方向是从下口进入,上口排出
C.实验中需要在蒸馏烧瓶中加入几粒碎瓷片,防止出现暴沸现象
D.蒸馏烧瓶必须垫石棉网
难度: 中等查看答案及解析
-
下列各项操作中,错误的是
A.用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液
B.进行分液时,分液漏斗中的下层液体从下口流出,上层液体从上口倒出
C.萃取分液前需对分液漏斗检漏
D.为保证分流漏斗内的液体顺利流出,需将上面的塞子拿下
难度: 中等查看答案及解析
-
下列实验装置或实验操作中错误的是
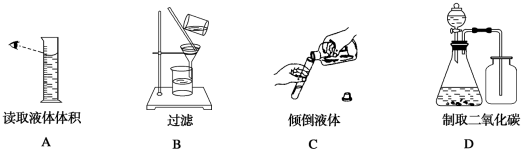
难度: 中等查看答案及解析
-
从下列混合物中分离出其中的一种成分,所采取的分离方法正确的是
A.由于碘在酒精中的溶解度大,可以用酒精把碘水中的碘萃取出来
B.水的沸点为100 ℃,酒精的沸点为78.5 ℃,所以可用加热蒸馏的方法使含水的酒精变为无水酒精
C.由于沙子和水不相溶,且存在明显的密度差异,因此可用过滤法分离沙子与水的混合物
D.NaCl的溶解度随温度下降而减小,可以用冷却法从热的含少量KNO3的NaCl浓溶液中分离得到纯净的NaCl
难度: 中等查看答案及解析
-
下列说法正确的是
A.1 mol任何气体所占体积都为22.4 L
B.1 mol H2O在标准状况下体积为22.4 L
C.1 mol气体体积为22.4 L,则一定是标准状况
D.气体摩尔体积不一定是22.4 L/mol
难度: 中等查看答案及解析
-
物质的量浓度相同的NaCl、MgCl2、AlCl3三种溶液,当溶液的体积比为3∶2∶1时,三种溶液中Cl−的物质的量之比为
A.1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.3∶4∶3
难度: 中等查看答案及解析
-
用98%的浓H2SO4(ρ=1.84 g/mL)配制1 mol/L的稀H2SO4100 mL,配制过程中可能用到下列仪器:
①100 mL量筒 ②10 mL量筒 ③50 mL烧杯 ④托盘天平 ⑤100 mL容量瓶 ⑥胶头滴管 ⑦玻璃棒。按使用时出现的先后顺序排列正确的是
A.②⑥③⑦⑤ B.④③⑤⑦⑥ C.①③⑦⑤⑥ D.②⑤⑦⑥
难度: 中等查看答案及解析
-
利用碳酸钠晶体(Na2CO3·10H2O)来配制0.5 mol/L的Na2CO3溶液1 000 mL,假如其他操作均是准确无误的,下列情况会引起配制溶液的浓度偏高的是
A.称取碳酸钠晶体100 g
B.定容时,俯视观察刻度线
C.移液时,对用于溶解碳酸钠晶体的烧杯没有进行冲洗
D.定容后,将容量瓶振荡均匀,静置时发现液面低于刻度线,于是又加入少量水至刻度线
难度: 中等查看答案及解析
-
标准状况下,现有①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述,其中不正确的是
A.体积:②>③>①>④ B.物质的量:②>③>④>①
C.质量:②>③>①>④ D.氢原子个数:①>③>④>②
难度: 中等查看答案及解析
-
同温、同压下,某容器充满O2重116 g,若充满CO2重122 g,现充满某气体重114 g,则该气体的相对分子质量为
A.28 B.60 C.32 D.44
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值,下列叙述正确的是
A.含有NA个原子的氢气在标准状况下的体积约为22.4 L
B.25 ℃,1.01×105 Pa下,64 g SO2中含有的原子数为3NA
C.40 g NaOH溶解在1 L水中,则其100 mL溶液中含Na+数为0.1NA
D.标准状况下,11.2 L CCl4含有的分子数为0.5NA
难度: 中等查看答案及解析
-
有甲、乙、丙三种溶液,进行如下操作:

则甲、乙、丙三种溶液中的溶质可能分别是
A.BaCl2、H2SO4、MgCl2 B.CaCl2、HNO3、AgNO3
C.CaCl2、HNO3、NaCl D.BaCl2、HCl、Na2CO3
难度: 中等查看答案及解析
-
有硫酸镁溶液500 mL,它的密度是1.20 g·cm−3,其中镁离子的质量分数是4.8%,则有关该溶液的说法不正确的是
A.溶质的质量分数是24% B.溶液的物质的量浓度是2.4 mol·L−1
C.溶质和溶剂的物质的量之比约为1∶21.1 D.硫酸根离子的质量是230.4 g
难度: 中等查看答案及解析