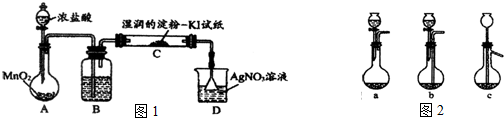
-
下列说法正确的是( )
A.硅肺病又称矽肺病,它是一种职业病,是人们长期吸入硅粉尘引起的
B.硝酸纤维、醋酸纤维以及常见的“六大纶”如腈纶、丙纶等都是化学合成的,所以又叫合成纤维
C.空气中的SO2主要来自化石燃料的燃烧,以及含硫矿石的冶炼和硫酸、磷肥厂产生的工业废气
D.煤可以经过气化和液化两物理变化过程,转化为清洁能源难度: 中等查看答案及解析
-
若NA表示阿伏加德罗常数的值,下列有关叙述不正确的是( )
A.常温下,28g乙烯与已烯混合物中所含共价键数目为6NA
B.1molNaHSO4熔化后阴阳离子数之和为3NA
C.2.0gD2O的中子数为NA
D.标况下22.4LNO与33.6LO2混合后气体分子数小于2.5NA电解难度: 中等查看答案及解析
-
下列离子反应方程式正确的是( )
A.用铁棒电极电解饱和食盐水:2Cl-+2H2O═2OH-+H2↑+Cl2↑
B.工业制漂白粉:Cl2+2OH-=Cl-+ClO-+H2O
C.向饱和Na2CO3溶液中通入CO2:2Na++CO32-+CO2+H2O═2NaHCO3↓
D.Ba(OH)2溶液中滴入NaHSO4溶液至恰好呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O难度: 中等查看答案及解析
-
目前工业上有一种方法是用CO2来生产燃料甲醇.为探究其反应原理,现进行如下实验,在体积为2L的密闭容器中,充入2mol CO2和6mol H2,一定条件下发生反应:CO2 (g)+3H2 (g)
CH3OH(g)+H2O(g);△H=-49.0kJ•mol-1,测得CO2和CH3OH(g)的浓度随时间变化如图所示,下列说法正确的是( )
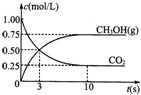
A.2molCO2和6molH2反应达到平衡时放热73.5kJ
B.从反应开始到平衡,CO2的平均速率v(CO2)=0.0325mol/
C.再充入1molCO2和3molH2,CO2的转化率不变
D.反应进行到3S时v(正)=v(逆)难度: 中等查看答案及解析
-
下列关系式不正确的是( )
A.常温下,pH=2的CH3COOH溶液与pH=12的NaOH溶液等体积混合后:c(CH3COOH)+c(H+)>c(OH-)
B.1L0.3mol•L-1NaOH溶液吸收标准状况下4.48LCO2:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
C.0.1mol•L-1的NH4Cl溶液与0.05mol•L-1的NaOH溶液等体积混合后:c(Cl-)>c(NH4-)>c(Na+)>c(OH-)>c(H+)
D.0.1mol•L-1的Na2CO3溶液中:c(CO32-)+c(HCO3-)+c(H2CO3)=0.1mol•L-1难度: 中等查看答案及解析
-
下列实验过程中产生的现象与对应的图形正确的是( )
A.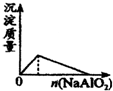 盐酸中加入NaAlO2溶液
盐酸中加入NaAlO2溶液
B.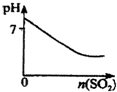 SO2气体通入溴水中
SO2气体通入溴水中
C.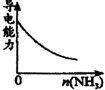 氨气通入醋酸溶液中
氨气通入醋酸溶液中
D.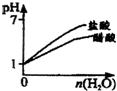 pH=1的醋酸和盐酸分别加水稀释
pH=1的醋酸和盐酸分别加水稀释 难度: 中等查看答案及解析
-
2010年12月1日,国务院总理温家宝来到四川凉山考察艾滋病防治工作.目前,艾滋病尚属国际医学难题,据研究,洋蓟素是一种新结构类型的抗艾滋病病毒的化合物,其结构如图所示,有关洋蓟素的说法正确的是( )
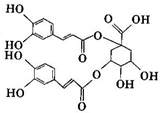
A.1mol该物质与足量钠反应生成3molH2
B.一定条件下能发酯化反应,消去反应,不能生水解发应
C.遇氯化铁生成紫色沉淀
D.1mol洋蓟素最多可与7molNaOH8mol溴水反应难度: 中等查看答案及解析
-
将一定量的镁和铜组成的混合物加入到稀HNO3中,金属完全溶解(假设反应中还原产物只有NO),向反应后的溶液中加入150mL一定浓度的NaOH溶液恰好沉淀完全,测得生成沉淀的质量比原合金的质量增加7.65g,则下列叙述中不正确的是( )
A.所用的NaOH溶液的物质的量浓度为3mol•L-1
B.当金属全部溶解时,收集到NO气体的体积一定为3.36L
C.参加反应的金属的总质量(m)为5.4g<m<14.4g
D.若将产生的气体全部转化为硝酸,则至少需要标况下2.52L的氧气难度: 中等查看答案及解析

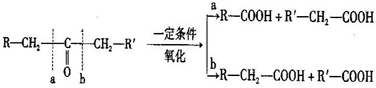
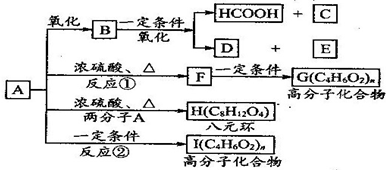 已知
已知