-
空气中最不活泼的成分是
A.氧气 B.氮气 C.二氧化碳 D.稀有气体
难度: 简单查看答案及解析
-
利用生物发光现象可检测“超微量钙”,此处“钙”是指
A.分子 B.原子 C.元素 D.单质
难度: 中等查看答案及解析
-
在空气中燃烧发出耀眼白光的是
A.氢气 B.木炭 C.镁带 D.硫粉
难度: 简单查看答案及解析
-
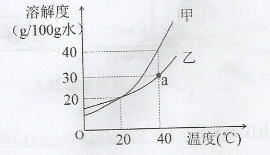
将饱和硝酸钾溶液变为不饱和溶液的操作是
A.降温 B.恒温蒸发水 C.加溶质 D.加水
难度: 简单查看答案及解析
-
过碳酸钠(Na2C2O4)可用于增加鱼塘内氧气含量,有关Na2C2O4的说法正确的是
A.它是混合物 B.它的焰色反应为黄色
C.它的摩尔质量是134 D.过碳酸钠制氧属于物理变化
难度: 中等查看答案及解析
-
能鉴别氢氧化钠溶液和氢氧化钙溶液的试剂是
A.酚酞试液 B.稀盐酸 C.碳酸钠溶液 D.硫酸铜溶液
难度: 中等查看答案及解析
-
电脑中大量使用硅,其元素符号是
A.Si B.S C.Ca D.Hg
难度: 简单查看答案及解析
-
表示两个氧分子的是
A.2O B.2O2 C.O D.O2
难度: 中等查看答案及解析
-
引起酸雨的主要物质是
A.PM2.5 B.SO2 C.CO2 D.N2
难度: 简单查看答案及解析
-
用于制造液晶电视的三氟化氮(NF3)中,氟元素为-1价,则氮元素的化合价为
A.0 B.-3 C.-1 D.+3
难度: 中等查看答案及解析
-
不能与稀盐酸反应的物质是
A.Ag B.Mg C.Al D.Fe2O3
难度: 简单查看答案及解析
-
加湿器可增加室内空气湿度,这是因为
A.分子体积很小 B.分子间有间隔
C.分子发生分解 D.分子不断运动
难度: 简单查看答案及解析
-
物质的俗名或主要成分与化学式不一致的是
A.烧碱:Na2CO3 B.天然气:CH4
C.生石灰:CaO D.干冰:CO2
难度: 简单查看答案及解析
-
正确的化学方程式是
A.4Fe +3O2
2Fe2O3
B.2NaOH + CO2 → NaCO3 + H2O
C.CaCO3
CaO + CO2↑
D.2NaOH + CuSO4 →Na2SO4 + Cu(OH)2
难度: 中等查看答案及解析
-
人类已能操纵原子制造分子,若用该方法制造葡糖糖(C6H12O6),不需要的原子是
A.氮原子 B.氧原子 C.氢原子 D.碳原子
难度: 简单查看答案及解析
-
工业炼锰的原理是3MnO2+4Al
3Mn+2Al2O3,其中二氧化锰作
A.催化剂 B.还原剂 C.氧化剂 D.干燥剂
难度: 中等查看答案及解析
-
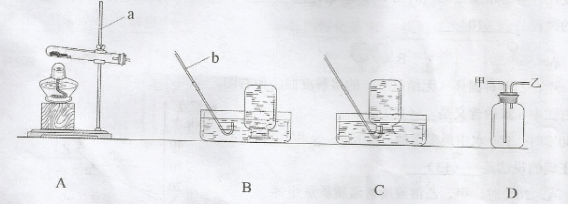
现有一包混有少量氯化钠的硝酸钾固体,通过如下实验提纯硝酸钾,其中错误的是

难度: 中等查看答案及解析
-
一包固体可能含有硫酸钠、氯化铜、碳酸钠和氯化钠中的一种或几种。根据以下实验得出的结 论错误的是

A.一定有硫酸钠 B.一定没有碳酸钠
C.可能有氯化钠 D.一定有氯化铜和氯化钠
难度: 困难查看答案及解析
-
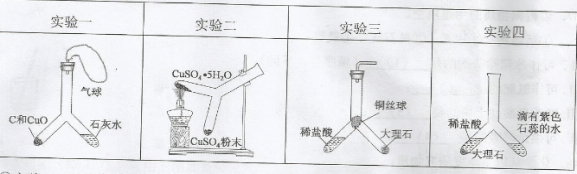
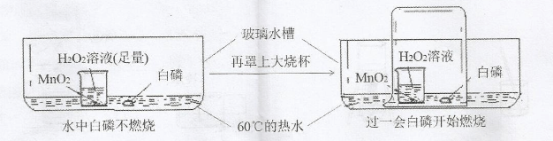
能达到实验目的的方案是

难度: 困难查看答案及解析
-
a、b可发生化合反应生成c。小辰做了两次该实验(每次均充分反应),反应前a和b的总质量都是9g,实验数据如下表。则m : n的值为
序号
反应前a的质量/g
反应前b的质量/g
反应后c的质量/g
实验①
7
2
6
实验②
m
n
9
A.5:4 B.2:7 C.1:2 D.2:1
难度: 困难查看答案及解析