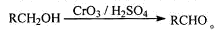-
下列说法正确的是
A.棉、麻、羊毛及合成纤维完全燃烧都只生成CO2和H2O
B.氨基酸、淀粉均属于高分子化合物
C.植物油的主要成分是高级脂肪酸
D.1mol
 最多能与5mo1 NaOH的水溶液完全反应
最多能与5mo1 NaOH的水溶液完全反应难度: 中等查看答案及解析
-
能在水溶液中大量共存的一组离子是
A.Na+、Mg2+、I-、ClO- B.Al3+、NH4+、SO42-、Cl-
C.K+、Ag+、NO3-、Cl- D.NH4+、Na+、OH-、SiO32-
难度: 困难查看答案及解析
-
设nA为阿伏加德罗常数的数值,下列说法正确的是
A.16g CH3OH中含有2nA个共价键
B.1 mol•L-1CuCl2溶液含有2nA个Cl-
C.1 mol Fe与足量的C12反应,转移3nA个电子
D.常温常压下,22.4L CH4中含有nA个CH4分子
难度: 中等查看答案及解析
-
用下图所示装置进行下列实验,放置一段时间后,实验结果与预测的现象不一致的是
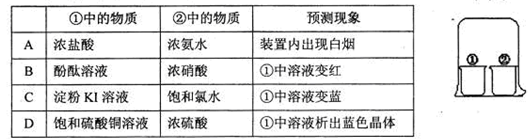
难度: 中等查看答案及解析
-
下列实验不能达到预期目的的是

A.利用I制取Fe(OH)2 B.利用II装置制取CH2=CH2
C.利用III装置进行铜与浓硝酸反应的实验 D.利用IV装置收集NH3
难度: 中等查看答案及解析
-
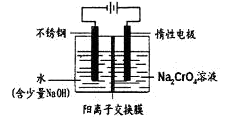
难挥发性二硫化担(TaS2)可采用如下装置提纯。将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中。反应如下:

下列说法正确的是
A.该反应的△H>0
B.在提纯过程中,S2的量不断增加
C.该反应的平衡常数与I2的浓度成正比
D.经过足够长时间后,石英管右端将得到纯净的TaS2
难度: 困难查看答案及解析
-
X、Y、Z、M、N五种主族元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。下列说法正确的是
A.原子半径:N>Z
B.单质的氧化性:Y>M
C.X、Z、M的氧化物均为共价化合物
D.M、N的最高价氧化物对应的水化物均属于强酸
难度: 困难查看答案及解析
-
醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是
A.醋酸溶液中:c(H+)>c(CH3COO-)>c(OH-)
B.NaHCO3溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)
C.等体积、等物质的量浓度的醋酸与氢氧化钠溶液混合:c(Na+)=c(CH3COO-)
D.中和等体积、等物质的量浓度的CH3COOH溶液和HCl溶液所消耗的NaOH物质的量相等
难度: 困难查看答案及解析