-
食醋、食盐和纯碱都是日常生活中常用的物质.食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸,是一种无色液体.食盐和纯碱都是白色固体.
(1)在用食醋拌凉菜时,往往可以闻到醋香,这说明醋酸具有______性.食醋不宜存放在含铁等金属的容器内,原因是______.请写一个你熟悉的酸与金属反应的化学方程式______.
(2)用食醋可以鉴别食盐和纯碱.请简要写出实验步骤和现象:______.
(3)纯碱的水溶液能使紫色石蕊溶液变蓝,说明其水溶液显______性,而在酸、碱、盐三类化合物中,纯碱属于______类.纯碱还能与许多化合物反应,请写一个你知道的纯碱与碱反应的化学方程式______.难度: 中等查看答案及解析
-
在“氢氧化钠的化学性质”实验探究课上,同学们做了氢氧化钠溶液与稀硫酸、氯化铜溶液之间反应的实验.为对本课产生的废液进行绿色排放,甲、乙两位同学对废液的成分进行探究和处理.请填空:
(1)甲同学取少量溶液样品,观察到样品澄清并呈浅蓝色.由此猜想,溶液中可能存在的离子为______.
(2)乙同学欲将废液处理为无色的中性溶液后再排放,他向废液中逐滴滴加氢氧化钠溶液,直至观察到______,说明废液达到了该同学的排放要求.难度: 中等查看答案及解析
-
下图是实验室常用的装置.请据图回答:
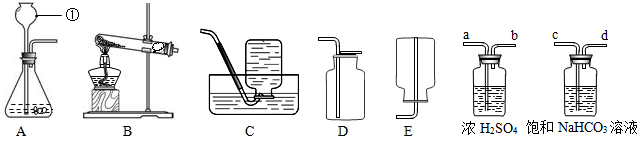
(1)写出仪器①的名称______.收集某气体只能采用E装置,由此推测该气体具有的性质______;
(2)用高锰酸钾制取氧气的装置组合是______(填序号),反应的化学方程式为______ K2MnO4+MnO2+O2↑难度: 中等查看答案及解析
-
下图是氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图,根据要求回答问题.

(1)铁的另两种常见氧化物的化学式是______、______.
(2)加水溶解过程中,在实验室里通常要使用的玻璃仪器有烧杯和______,操作A的名称是______.
(3 )副产品P是______,由溶液N获得该副产品的操作顺序是b→______→______→d.
a.过滤 b.加热浓缩 c.冷却结晶 d.晶体加热至完全失去结晶水
(4)通空气时的化学方程式是4Fe(OH)2+2H2O+O2═4Fe(OH)3,由沉淀M获得Fe3O4的过程中发生的反应为Fe(OH)2+2Fe(OH)3Fe3O4+4H2O,控制“一定量空气”的目的是______,沉淀M中Fe(OH)2和Fe(OH)3的最佳质量比为______.
(相对分子质量:Fe(OH)2-90,Fe(OH)3-107)难度: 中等查看答案及解析
-
将50gCaCl2溶液与77gNa2CO3溶液混合后,恰好完全反应,过滤、洗涤、烘干后,得到10g白色固体.请计算:
(1)CaCl2溶液中溶质的质量为______g.
(2)过滤后所得溶液中溶质的质量分数.(写出计算过程)难度: 中等查看答案及解析

