-
t℃时,向一支盛有0.15g熟石灰的烧杯中加入50g水,充分振荡后静置,烧杯底部仍有未溶解的白色固体.下列相关叙述正确的是( )
A.升高温度上层清液变为不饱和溶液
B.t℃时,熟石灰的溶解度为0.3 g
C.烧杯中溶液的质量小于50.15 g
D.上层清液中溶质质量分数大于0.3%
难度: 简单查看答案及解析
-
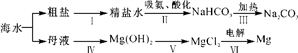
下列属于物理变化的是( )
A.海水晒盐
B.海水制“碱”
C.海水制镁
D.除去海水中的氯化镁等可溶性杂质
难度: 中等查看答案及解析
-
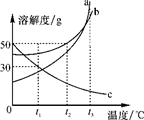
如图是硝酸钾的溶解度曲线,下列说法错误的是

A.硝酸钾的溶解度随温度的升高而增大
B.降低温度可以使接近饱和的硝酸钾溶液变饱和
C.60℃时120g硝酸钾与100g水充分混合可以形成饱和溶液
D.60℃时硝酸钾溶液中溶质质量分数一定大于30℃时硝酸钾溶液中溶质质量分数
难度: 困难查看答案及解析
-
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量的某物质X,溶液的pH随滴入X的量的变化关系如下图所示,则X可能是

A.水
B.纯碱溶液
C.澄清石灰石
D.稀盐酸
难度: 困难查看答案及解析