-
下列物质能导电,而且属于电解质的是
A.水银 B.无水乙醇 C.氯化钠溶液 D.熔融的硫酸铜
难度: 简单查看答案及解析
-
“纳米材料”是粒子直径为1~100 nm(纳米)的材料,纳米碳就是其中的一种。若将纳米碳均匀地分散到蒸馏水中,所形成的分散系
①是溶液 ②是胶体 ③能产生丁达尔效应 ④能透过滤纸 ⑤不能透过滤纸
⑥静置后,会析出黑色沉淀
A.①④⑥ B.②③④ C.②③⑤ D.②③④⑥
难度: 简单查看答案及解析
-
下列物质中,不属于合金的是
A.硬铝 B.黄铜 C.金箔 D.钢铁
难度: 简单查看答案及解析
-
下列说法正确的是
A.氢氧化钠溶液应保存在带磨砂玻璃塞的无色细口瓶中
B.硅是制造光导纤维的材料
C.水玻璃可用作木材防火剂
D.水晶是一种无色,坚硬难熔的硅酸盐
难度: 简单查看答案及解析
-
配制100mL0.5mol/LNaOH溶液的操作有 ①计算 ②冷却 ③洗涤 ④溶解 ⑤转移 ⑥称量 ⑦定容,次序正确的是
A.①⑥③②⑤④⑦ B.①⑥④⑤②③⑦
C.①⑥④②⑤③⑦ D.①⑥③④⑤②⑦
难度: 简单查看答案及解析
-
食盐溶液中存在Ca2+、Mg2+、SO42-等杂质,除杂时加入NaOH、Na2CO3、BaCl2和盐酸,下列添加试剂顺序正确的有
①NaOH BaCl2 Na2CO3 HCl ②BaCl2 HCl NaOH Na2CO3
③Na2CO3 BaCl2 NaOH HCl ④BaCl2 NaOH Na2CO3 HCl
A.①③ B.①④ C.③④ D.①③④
难度: 简单查看答案及解析
-
实验室里需用480mL 0.1 mol/L的硫酸铜溶液,以下操作正确的是
A.称取7.68g硫酸铜,加入500mL水 B.称取12.0g胆矾配成500mL溶液
C.称取8.0g硫酸铜,加入500mL水 D.称取12.5g胆矾配成500mL溶液
难度: 简单查看答案及解析
-
下列溶液中能用来区别SO2和CO2气体的是
①澄清的石灰水 ②氢硫酸 ③氯水 ④酸性高锰酸钾溶液 ⑤氯化钡溶液 ⑥品红溶液
A.①④⑤⑥ B.②③④⑤ C.①②③⑥ D.②③④⑥
难度: 简单查看答案及解析
-
根据反应式:①2Fe3+ + 2I- = 2Fe2+ + I2 ②Br2 + 2Fe2+ ="==" 2Fe3+ +2Br-,可判断离子的还原性从强到弱的顺序是
A.Br-、Fe2+、I- B.I-、Fe2+、Br-
C.Br-、I-、Fe2+ D.Fe2+、I-、Br-
难度: 简单查看答案及解析
-
现有下列五个转化,其中不能通过一步反应实现的是
①SiO2→Na2SiO3;②CuSO4→CuCl2;③SiO2→H2SiO3;④CuO→Cu(OH)2;⑤Na2O2→Na2SO4
A.①② B.③④ C.②③④ D.②③④⑤
难度: 简单查看答案及解析
-
一定条件下硝酸铵受热分解的未配平化学方程式为:NH4NO3 - HNO3+N2+H2O,在反应中被氧化与被还原的氮原子数之比为
A.5∶3 B.5∶4 C.1∶1 D.3∶5
难度: 简单查看答案及解析
-
在某无色溶液中缓慢地滴入NaOH溶液直至过量,产生沉淀的质量与加入的NaOH溶液体积的关系如右图所示,由此确定,原溶液中可能含有的阳离子是
A.Mg2+、Al3+、Fe2+ B.H+、Mg2+、Al3+
C.H+、Ba2+、Al3+ D.只有Mg2+、Al3+
难度: 简单查看答案及解析
-
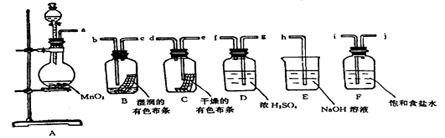
如图,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象;当打开B阀后,C处红布条逐渐褪色。则D瓶中装的是
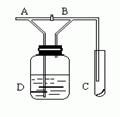
A.浓盐酸 B.NaOH溶液 C.H2O D.饱和NaCl溶液
难度: 简单查看答案及解析
-
下列有关实验的操作及描述正确的是
A.可以利用烧碱溶液除去混在MgO中的Al2O3
B.用四氯化碳萃取碘水中的碘单质,上层显紫红色
C.将Fe(OH)3沉淀溶于沸水可制得Fe(OH)3胶体
D.测定Na2CO3溶液的pH值,操作时应将先pH试纸润湿
难度: 简单查看答案及解析
-
在FeCl3、CuCl2和HCl的混合液中加入铁粉,待反应结束,所剩固体滤出后不能被磁铁吸引,则反应后溶液不可能大量存在的阳离子是
A.H+ B.Fe3+ C.Fe2+ D.Cu2+
难度: 简单查看答案及解析
-
关于Na2CO3和NaHCO3两种白色固体的性质比较,下列叙述正确的是
A.固体状态下,Na2CO3比NaHCO3稳定
B.Na2CO3比NaHCO3更难溶于水
C.配制两者等物质的量浓度的溶液,Na2CO3比NaHCO3的碱性强
D.向两者等物质的量浓度的溶液中加入等量的稀盐酸,Na2CO3比NaHCO3反应快
难度: 简单查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是
A.标准状况下,22.4L H2含有的分子数为NA
B.18g H2O在标准状况下的体积是22.4L
C.常温常压下,1.6g CH4含有的电子数为NA
D.物质的量浓度为0.5mol /L的MgCl2溶液中,含有Cl–个数为 NA
难度: 简单查看答案及解析
-
某无色溶液能与铝作用生成氢气,则该溶液可能是下列哪一个离子组
A.H+、Ba2+、Mg2+、C1— B.C1—、CO32—、NO3—、Mg2+
C.Cu2+、SO42—、K+、H+ D.NO3—、OH—、Ba2+、C1—
难度: 简单查看答案及解析
-
下列离子方程式正确的是
A.钠与水反应:Na + 2H2O ="=" Na+ + 2OH— + H2↑
B.铝片溶于氢氧化钠溶液中:2Al + 2OH— + 2H2O ="=" 2A1O2— + 3H2↑
C.氯化亚铁与氯水:Fe2+ + C12 ="=" Fe3+ + 2C1—
D.纯碱与稀盐酸反应:CO32— + 2H+ == H2O + CO2↑
难度: 简单查看答案及解析
-
关于下列各装置图的叙述中,正确的是
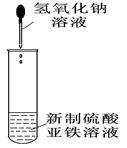

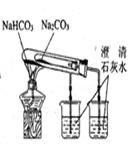
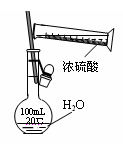
① ② ③ ④
A.利用装置①可制备氢氧化亚铁并长时间观察其颜色
B.装置②中X若为四氯化碳,可用于吸收HCl气体,并防止倒吸
C.装置③无法验证Na2CO3和NaHCO3两种固体的热稳定性
D.通过④的方法配制一定浓度的稀硫酸溶液
难度: 简单查看答案及解析