-
下列说法错误的是( )。
A.含有共价键的化合物一定是共价化合物
B.在共价化合物中一定含有共价键
C.含有离子键的化合物一定是离子化合物
D.双原子单质分子中的共价健一定是非极性键
难度: 中等查看答案及解析
-
制备氯乙烷的方法合理的是( )
A. 乙烯与氯化氢加成 B. 等量的乙烷与氯气取代
C. 乙烯与氯气加成 D. 乙烯加氢后再氯代
难度: 中等查看答案及解析
-
下列各组有机物中,其一氯代物的数目不相等的是( )
A. 正戊烷和正己烷 B. 新戊烷和2-甲基丙烷
C. 环戊烷和乙烷 D. 丙烷和2,3-二甲基丁烷
难度: 简单查看答案及解析
-
下列粒子半径最小的是( )。
A. Na+ B. Na C. Cl D. Cl-
难度: 简单查看答案及解析
-
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物均呈碱性,且碱性B>A,C和D的气态氢化物的稳定性C>D;E是这五种元素中原子半径最小的元素,则它们的原子序数由小到大的顺序是( )。
A. A、B、C、D、E B. E、C、D、B、A
C. B、A、D、C、E D. C、D、A、B、E
难度: 简单查看答案及解析
-
铊是超导材料的组成元素之一,铊在周期表中位于第六周期,与铝是同族元素,元素符号是Tl,以下对铊的性质的推断不正确的是( )
A. 铊是易导电的银白色金属 B. 能生成+3价离子化合物
C. Tl(OH)3是两性氢氧化物 D. Tl3+的氧化能力比Al3+弱
难度: 中等查看答案及解析
-
下列各组化合物的性质比较,不正确的是 ( )
A. 酸性: HClO4 > HBrO4 > HIO4 B. 碱性: NaOH > Mg(OH)2> Al(OH)3
C. 稳定性: PH3> H2S > HCl D. 非金属性:F > O > S
难度: 中等查看答案及解析
-
在一定条件下,RO3-与R-可发生反应:RO3-+5R-+6H+===3R2+3H2O,下列关于R元素的叙述中,正确的是( )
A. 元素R位于周期表中第ⅤA族
B. RO3-中的R只能被还原
C. R2在常温常压下一定是气体
D. 若1 mol RO3-参与该反应,则转移的电子的物质的量为5 mol
难度: 中等查看答案及解析
-
某粒子含有6个电子、7个中子,呈电中性,则它的化学符号可能是( )
A. 13Al B. 13Al C. 13C D. 13C
难度: 简单查看答案及解析
-
下列物质的电子式书写正确的是( )

A. A B. B C. C D. D
难度: 中等查看答案及解析
-
与丙烯具有相同的碳、氢百分含量,但既不是同系物又不是同分异构体的是( )
A.环丙烷 B.环丁烷 C.乙烯 D.丙烷
难度: 简单查看答案及解析
-
下列物质的沸点按由高到低的顺序排列正确的是( )
①CH3(CH2)2CH3②CH3(CH2)3CH3③(CH3)3CH ④(CH3)2CHCH2CH3
A. ②④①③ B. ④②①③ C. ④③②① D. ②④③①
难度: 中等查看答案及解析
-
下列说法正确的是
A. 原子最外层电子数等于或大于3(小于8)的元素一定是非金属元素
B. 原子最外层只有1个电子的元素一定是金属元素
C. 原子最外层电子数比次外层电子数多的元素一定位于第二周期
D. 某元素的离子最外层电子数与次外层电子数相同,该元素一定位于第三周期
难度: 中等查看答案及解析
-
aXn-和bYm+ 为两主族元素的离子,它们的电子层结构相同,下列判断错误的是
A. 原子半径X<Y B. a+n=b-m
C. Y最高价氧化物的化学式为YOm D. Xn-离子的半径大于Ym+ 离子的半径
难度: 中等查看答案及解析
-
右下表为元素周期表前四周期的一部分,下列有关R、W、X、Y、Z五种元素的叙述中,正确的是( )。
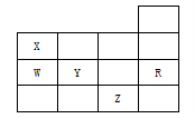
A. 常压下五种元素的单质中,Z单质的沸点最高
B. Y、Z的阴离子电子层结构都与R原子的相同
C. Y的氢化物的沸点比H2O的沸点高
D. Y元素的非金属性比W元素的非金属性强
难度: 中等查看答案及解析
-
下列说法中,正确的是( )
A. 符合通式CnH2n的烃一定是同系物
B.
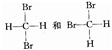 是同分异构体
是同分异构体C. 乙烯使酸性KMnO4溶液褪色是加成反应
D. 由丙烯生成聚丙烯是聚合反应
难度: 简单查看答案及解析
-
在催化剂作用下,200mL的某烷烃与某炔烃的混合气体与氢气发生加成反应,最多需要100mL的氢气(同温同压),则混和气体中烷烃与炔烃的物质的量之比为( )
A. 1∶1 B. 1∶2
C. 1∶3 D. 3∶1
难度: 简单查看答案及解析