-
下列为人体提供能量的营养物质中,属于高分子化合物的是
A. 淀粉 B. 蔗糖 C. 果糖 D. 葡萄糖
难度: 简单查看答案及解析
-
下列物质中,含有共价键的离子化合物是
A. NH3 B. HCl C. NaOH D. NaCl
难度: 中等查看答案及解析
-
C-NMR(核磁共振)可以用于含碳化合物的结构分析有关
C的说法正确的是
A. 质子数为6 B. 电子数为13 C. 中子数为6 D. 质量数为6
难度: 简单查看答案及解析
-
下列过程属于物理变化的是
A. 煤旳干馏 B. 煤旳气化 C. 石油分馏 D. 石油裂化
难度: 中等查看答案及解析
-
在下列影响化学反应速率的因素中,能使化学反应速率加快的方法是( )
①升高温度 ②加入催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末
A. ①②③ B. ①②④ C. ①③④ D. ①②③④
难度: 简单查看答案及解析
-
CO、NO及H2S都是有毒气体。下列有关这三种气体的说法正确的是 ( )
A. 都能与氧气反应 B. 都易溶于水
C. 都能与碱溶液反应 D. 都是电解质
难度: 简单查看答案及解析
-
分类方法广泛适用于化学科学中,以下物质分类不正确的是
A.纯金属与合金均属于金属材料
B.纯碱和烧碱的水溶液均显示碱性,故均属于碱类
C.按分散质的粒子直径大小可将分散系分为溶液、浊液和胶体
D.溶于水后其水溶液能导电化合物不一定是电解质
难度: 中等查看答案及解析
-
下列递变规律正确的是 ( )
A. Na、Mg、Al的金属性依次减弱
B. P、S、Cl元素的最高正价依次降低
C. Al3+、Mg2+、Na+的离子半径依次减小
D. HNO3、H3PO4、H2SO4的酸性依次增强
难度: 中等查看答案及解析
-
相同质量的铝分别投入足量的下列物质中反应生成氢气,消耗溶质物质的量最少的是
A. 稀硫酸 B. 稀盐酸 C. 氢氧化钡溶液 D. 氢氧化钠溶液
难度: 简单查看答案及解析
-
一定条件下密闭容器中发生如下反应:N2(g)+3H2(g)
2NH3(g),能说明该反应达到化学平衡状态的是( )
A. N2、H2、NH3的浓度相等 B. N2、H2、NH3的浓度不再变化
C. N2、H2、NH3在密闭容器中共存 D. 反应停止,正、逆反应速率都等于零
难度: 中等查看答案及解析
-
已知反应A+B= C+D的能量变化如下图所示,下列说法正确的是
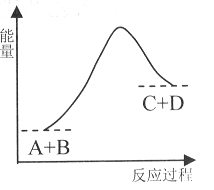
A. 该反应是放热反应
B. 只有在加热条件下才能进行
C. 反应物的总能量高于生成物的总能量
D. 反应中断开化学键吸收的总能量高于形成化学键放出的总能量
难度: 简单查看答案及解析
-
等质量的下列有机物完全燃烧,消耗O2最多的是( )
A. CH4 B. CH3CH3 C. C2H2 D. C5H12
难度: 中等查看答案及解析
-
化学中存在一些守恒或平衡原理,下列叙述正确的是
A. 根据质量(原子)守恒定律,某物质完全燃烧的产物是CO2和H2O则该物质一定是烃
B. 根据能量守恒定律,所有化学反应的反应物的总能量一定等于生成物的总能量
C. 根据电子守恒定律,原电池中负极反应失电子数一定等于正极反应得电子数
D. 根据化学平衡原理,可逆反应的正反应速率在任何时刻一定等于逆反应速率
难度: 中等查看答案及解析
-
X元素的阳离子和Y元素的阴离子具有与氖原子相同的电子层结构,下列说法正确的是
A. 原子序数:X<Y
B. 原子半径:X>Y
C. 原子的最外层电子数:X>Y
D. 得电子能力:X>Y
难度: 简单查看答案及解析
-
把甲、乙、丙、丁四块金属泡在稀H2SO4中,用导线两两相连可以组成各种原电池。若甲、乙相连,甲为负极;丙、丁相连,丁上有气泡逸出;甲、丙相连,甲上发生氧化反应;乙、丁相连,乙是电子流入的一极。则四种一金属的活动性顺序由大到小排列为
A. 甲>丙>丁>乙 B. 甲>丙>乙>丁
C. 甲>乙>丙>丁 D. 乙>丁>丙>甲
难度: 简单查看答案及解析
-
如图W、X、Y、Z为四种物质,若箭头表示能一步转化的常见反应,其中常温下能实现图示转化关系的是
选项
W
X
Y
Z
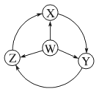
A
S
SO2
SO3
H2SO4
B
Na
Na2O2
NaOH
NaCl
C
Fe
FeCl3
Fe(OH)2
FeCl2
D
Al
AlCl3
Na[Al(OH)4]
Al2(SO4)3
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
设NA为阿伏加德罗常数的值。下列说法正确的是
A. 常温、常压下,18g H2O含有的原子数为3 NA
B. 标准状况下,2.24 L乙醇含有的分子数为0.1 NA
C. 1 L 1.0 mol·L—1 K2SO4溶液中含有的K+数为NA
D. 标准状况下,2.24 L氦气和2.24L氧气所含的原子数均为0.2NA
难度: 简单查看答案及解析
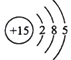 (核内15个中子)
(核内15个中子)