-
中国传统文化中的成语是中华民族智慧的结晶,下列成语描绘的变化属于化学变化的是( )
A. 刻舟求剑 B. 百炼成钢 C. 拨云见日 D. 量体裁衣
难度: 简单查看答案及解析
-
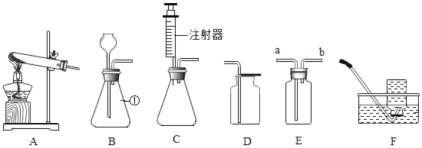
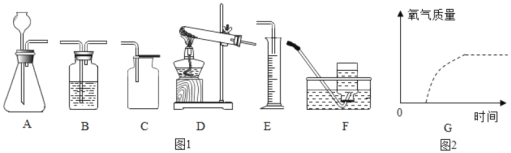
化学是一门以实验为基础的科学,下列实验操作错误的是( )
A.
 量取一定量的液体 B.
量取一定量的液体 B.  取用氯化钠溶液
取用氯化钠溶液C.
 检查气密性 D.
检查气密性 D.  氧气的验满
氧气的验满难度: 简单查看答案及解析
-
如图为测定空气中氧气含量的实验装置,下列做法合理的是( )
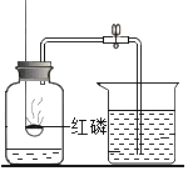
A. 用过量的红磷进行实验
B. 红磷点燃后,缓慢伸入瓶中并塞紧橡皮塞
C. 红磷熄灭后,立即打开止水夹
D. 用蜡烛代替红磷进行实验
难度: 简单查看答案及解析
-
观察实验现象是实验探究活动中重要的环节,下列有关物质燃烧现象描述正确的是( )
A. 铁丝在氧气中燃烧:火星四射,生成四氧化三铁
B. 红磷在空气中燃烧:产生大量的白色烟雾,放出大量的热
C. 硫粉在空气中燃烧:产生淡蓝色火焰,生成一种刺激性气味的气体
D. 木炭在氧气中燃烧:发出白光,产生一种刺激性气味的气体
难度: 简单查看答案及解析
-
如图是一氧化碳与氧气反应的微观模型图,如图是该化学反应的微观过程(图中“
”表示氧原子,“
”表示碳原子)。下列说法错误的是( )

A. 反应中所有物质都是由分子构成
B. 反应前后原子的数目没有发生变化
C. 反应前后原子的种类没有发生变化
D. 反应前后分子的数目和种类都没有变
难度: 简单查看答案及解析
-
2018年中美贸易摩擦波及手机芯片。芯片是内含集成电路的硅片,如图是硅元素在元素周期表中的相关信息,下列说法不正确的是( )
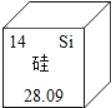
A. 该元素原子的质子数为14
B. 硅元素是地壳中含量最高的元素
C. 硅元素的相对原子质量为28.09
D. 硅原子的原子核外有14个电子
难度: 简单查看答案及解析
-
如图是关于氧气化学性质的部分知识网络,关于该图说法正确的是( )

A. Ⅰ、Ⅱ两类反应均体现了氧气的氧化性
B. Ⅰ、Ⅱ中的反应类型都是化合反应
C. Ⅰ类反应放出热量,Ⅱ类反应吸收热量
D. Ⅰ、Ⅱ两类反应均会发光
难度: 简单查看答案及解析
-
2018年六五环境日主题是“美丽中国,我是行动者”。生态环境部确立该主题,旨在推动社会各界和公众积极参与生态文明建设,携手行动,共建天蓝、地绿、水清的美丽中国。下列说法正确的是( )
A. 改进燃煤锅炉烟囱,将废气排到高空,可以减少环境污染
B. 淡水资源是取之不尽、用之不竭的
C. 工业废水和生活污水达标后再排放
D. 海洋有自净能力,所以不存在海水污染问题
难度: 简单查看答案及解析
-
分析推理是化学学习中常用的思维方法。下列分析推理说法正确的是( )
A. 分子可以构成物质,但物质不一定都是分子构成
B. 离子是带电的粒子,所以带电的粒子一定是离子
C. 水和过氧化氢的组成元素相同,则两者的化学性质相同
D. 水电解产生氢气和氧气,所以水是由氢气和氧气组成的
难度: 简单查看答案及解析
-
2018年10月16日华为发布新款手机,高密度大容量电池和超级快充技术,举世瞩目。一种新型的高能手机锂电池的总反应式可表示为:Li+MnO2═LiMnO2下列说法正确的是( )
A. 该反应属于分解反应
B. MnO2在该反应中作为催化剂
C. 锂原子容易得到电子
D. 给电池充电时化学能转化为电能
难度: 简单查看答案及解析