-
下列叙述中不正确的是( )
A. 钠在反应TiCl4+4Na===Ti+4NaCl中作还原剂
B. NaOH应密封保存,以防分解变质
C. 盛放KOH溶液的试剂瓶不能用玻璃塞
D. 当足量的CO2通入饱和NaOH溶液中,会有固体析出
难度: 中等查看答案及解析
-
下列做法不正确的是( )
A. Na2O2用作呼吸面具的供氧剂
B. NaHCO3的热稳定性大于Na2CO3
C. 乙醇可与金属钠反应放出氢气
D. 金属钠着火时,用细沙覆盖灭火
难度: 中等查看答案及解析
-
等质量的钠进行下列实验,其中生成氢气最多的是( )
A. 将钠投入到足量水中
B. 将钠用铝箔包好并刺一些小孔,再放入足量的水中
C. 将钠放入足量稀硫酸中
D. 将钠放入足量稀盐酸中
难度: 中等查看答案及解析
-
下列说法正确的是( )
A. Na2O2遇到湿润的紫色石蕊试纸后,石蕊试纸最终变成蓝色
B. Na2O2与CO2反应生成0.1 mol O2时转移电子0.4 mol
C. Na2O2投入到CuCl2溶液中有蓝色沉淀及气泡产生
D. 向饱和烧碱溶液中加入2 g Na2O2,充分反应完后,溶液中c(Na+)不变
难度: 中等查看答案及解析
-
某工厂用提取粗盐后的盐卤(主要成分为MgCl2)制备金属镁,其工艺流程如下。
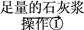
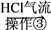
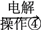
,下列说法错误的是( )
A. 在实验室实施操作①需要的玻璃仪器是漏斗、烧杯、玻璃棒
B. Mg(OH)2―→MgCl2的离子方程式为:Mg(OH)2+2H+===Mg2++2H2O
C. 操作②是将MgCl2溶液蒸干后冷却结晶
D. 操作④阴极和阳极产物的质量比是24∶71
难度: 中等查看答案及解析
-
向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸。下列离子方程式与事实不相符的是( )
A. OH-+CO
+2H+===HCO
+H2O
B. 2OH-+CO
+3H+===HCO
+2H2O
C. 2OH-+CO
+4H+===CO2↑+3H2O
D. OH-+CO
+3H+===CO2↑+2H2O
难度: 困难查看答案及解析
-
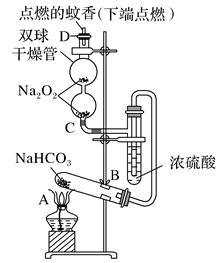
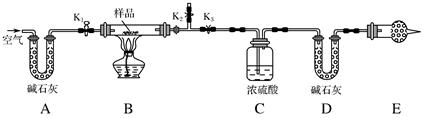
用如图所示实验装置进行相关实验探究,其中装置不合理的是( )
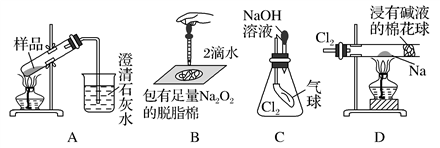
A. 鉴别纯碱与小苏打
B. 证明Na2O2与水反应放热
C. 证明Cl2能与烧碱溶液反应
D. 探究钠与Cl2反应
难度: 中等查看答案及解析
-
X、Y、Z、W四种物质的转化关系如图所示。下列组合中不符合该关系的是( )
A
B
C
D
X
HCl
Na2O2
Na2CO3
SO2
Y
FeCl2
NaOH
CO2
Na2SO3
Z
Cl2
Na2CO3
CaCO3
H2SO4
W
FeCl3
NaHCO3
Ca(HCO3)2
NaHSO3
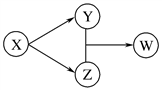
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
有关NaHCO3和Na2CO3的性质,以下叙述错误的是( )
A. 等质量的NaHCO3和Na2CO3与足量盐酸反应,在相同条件下Na2CO3产生的CO2体积小
B. 等物质
的量的两种盐与同浓度盐酸完全反应,所消耗盐酸的体积Na2CO3是NaHCO3的两倍
C. 等质量NaHCO3和Na2CO3与盐酸完全反应,前者消耗盐酸较多
D. 等物质的量的NaHCO3和Na2CO3与足量盐酸反应产生CO2一样多
难度: 中等查看答案及解析
-
向四只盛有一定量NaOH溶液的烧杯中通入不同量的CO2气体,再在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图(忽略CO2的溶解和HCl的挥发):
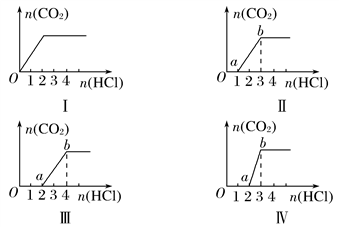
则下列分析都正确的组合是( )①Ⅰ图对应溶液中的溶质为NaHCO3
②Ⅱ图对应溶液中的溶质为Na2CO3和NaHCO3,且二者的物质的量之比为1∶1
③Ⅲ图对应溶液中的溶质为NaOH和Na2CO3,且二者的物质的量之比为1∶1
④Ⅳ图对应溶液中的溶质为Na2CO3
A. ①② B. ①③
C. ②④ D. ②③
难度: 中等查看答案及解析
-
用光洁的铂丝蘸取某无色溶液在无色火焰上灼烧,直接观察到火焰呈黄色,下列各判断正确的是( )
A. 只含有Na+
B. 一定含有Na+,可能含有K+
C. 既含有Na+,又含有K+
D. 可能含有Na+,可能还含有K+
难度: 中等查看答案及解析
-
为精确测定工业纯碱中碳酸钠的质量分数(含少量NaCl),准确称量W0 g样品进行实验,下列实验方法所对应的实验方案和测量数据合理(除W0外)的是( )
选项
实验方法
实验方案
测量数据
A
滴定法
将样品配成100 mL溶液,取10 mL,加入酚酞,用标准盐酸滴定
消耗盐酸
的体积
B
量气法
将样品与盐酸反应,生成的气体全部被碱石灰吸收
碱石灰
增重
C
重量法
样品放入烧瓶中,置于电子天平上,加入足量盐酸
减轻的
质量
D
量气法
将样品与盐酸反应,气体通过排水量气装置量气
排水体积
A. A B. B C. C D. D
难度: 中等查看答案及解析