-
下列有关实验的说法错误的是( )
A. 在蒸馏实验中,温度计的水银球位于支管口处是为了测出馏分的沸点
B. 用结晶法分离硝酸钾和氯化钠的混合物,用分液法分离水和硝基苯的混合物
C. 在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的损失
D. 作为重结晶实验的溶剂,杂质在此溶液中的溶解度受温度影响应该很大
难度: 中等查看答案及解析
-
化学与人类生活密切相关,下列说法错误的是( )
A.苯酚有一定毒性,可以作消毒剂和防腐剂
B.油脂皂化生成的高级脂肪酸钠是肥皂的有效成分
C.用食醋去除水壶中的水垢时所发生的是水解反应
D.木糖醇是一种新型的甜味剂,适合糖尿病患者的需要
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 乙烯和聚乙烯均能使溴水褪色
B. 甲烷、苯和油脂均不能使酸性KMnO4溶液褪色
C. 乙酸和乙酸乙酯均能发生取代反应
D. 蔗糖和麦芽糖是同分异构体,均可以水解且产物相同
难度: 简单查看答案及解析
-
下列有机实验操作或叙述正确的是( )。
A. 实验室配制银氨溶液时,应将2%硝酸银滴入2mL 2%的氨水中
B. 除去乙酸乙酯中的部分乙醇和乙酸可用饱和Na2CO3溶液
C. 卤代烃和酯的水解都可用浓硫酸作催化剂
D. 在卤代烃水解后的溶液中加入硝酸银溶液观察沉淀现象就可确定其中的卤素
难度: 简单查看答案及解析
-
为了除去粗盐中的CaCl2、MgCl2、Na2SO4及泥沙,可将粗盐溶于水,通过如下几个实验步骤,可制得纯净的食盐水:①加入稍过量的Na2CO3溶液;②加入稍过量的NaOH溶液;③加入稍过量的BaCl2溶液;④滴入稀盐酸至无气泡产生;⑤过滤。不正确的操作顺序是
A. ⑤②①③⑤④ B. ⑤③①②⑤④ C. ⑤②③①⑤④ D. ⑤③②①⑤④
难度: 中等查看答案及解析
-
5个碳的烷烃的同分异构体共有( )
A. 1种 B. 2种 C. 3种 D. 4种
难度: 中等查看答案及解析
-
根据有机化合物的命名原则,下列命名正确的是
A.
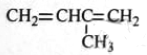 3-甲基-1,3-丁二烯
3-甲基-1,3-丁二烯B.
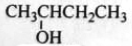 2-羟基丁烷
2-羟基丁烷C. CH3CH(C2H5)CH2CH2CH32-乙基戊烷
D. CH3CH(NH2)CH2COOH3-氨基丁酸
难度: 中等查看答案及解析
-
将CH3COOH和H18O—C2H5混合加热发生酯化反应,已知酯化反应是可逆反应,反应达到平衡后,下列说法正确的是
A. 18O存在于所有物质里 B. 18O仅存在于乙醇和乙酸乙酯里
C. 18O仅存在于乙醇和水里 D. 有的乙醇分子可能不含18O
难度: 中等查看答案及解析
-
等质量的铜片,在酒精灯上加热后,分别插入下列溶液中,放置片刻后取出,铜片质量比加热前增加的是
A. 硝酸 B. 无水乙醇
C. 石灰水 D. 盐酸
难度: 中等查看答案及解析
-
某有机物的分子式为C5H10O,它能发生银镜反应和加成反应;若将它与H2加成,所得产物的结构简式可能是( )
A. (CH3)3CCH2OH B. (CH3CH2)2CHOH
C. CH3(CH2)2CHOHCH3 D. CH3CH2C(CH3)2OH
难度: 简单查看答案及解析
-
欲从苯酚的乙醇溶液中分离苯酚和乙醇,有下列操作:①蒸馏;②过滤;③静置分液;④加入足量的金属钠;⑤通入过量的二氧化碳;⑥加入足量的NaOH溶液;⑦加入足量的FeCl3溶液;⑧加入乙酸和浓硫酸的混合液加热。合理的实验操作步骤及顺序是( )
A. ④⑤③ B. ⑥①⑤③
C. ⑧①⑦③ D. ⑤②⑥③
难度: 简单查看答案及解析
-
下列反应中属于取代反应的是( )
A. 2CH4
C2H4+2H2 B. H2+Cl2═2HCl
C. C2H5Cl+Cl2
C2H4Cl2+HCl D. CH4+2O2
CO2+2H2O
难度: 中等查看答案及解析
-
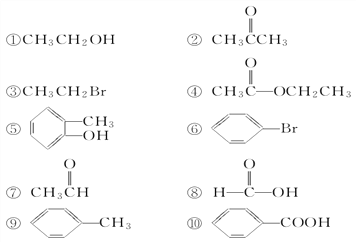
纳米分子机器日益受到关注,机器常用的“车轮”组件结构如下图所示,下列说法正确的是( )
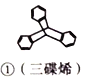
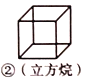


A. ①②③ ④均属于烃 B. ①③均属于苯的同系物
C. ②④的二氯代物物分别有3种和6种 D. ①②③均能发生取代反应
难度: 中等查看答案及解析
-
下列图示的四种实验操作名称从左到右依次是

A. 过滤、蒸发、蒸馏、萃取 B. 过滤、蒸馏、蒸发、萃取
C. 蒸发、蒸馏、过滤、萃取 D. 萃取、蒸馏、蒸发、过滤
难度: 简单查看答案及解析
-
某烯烃
只含1个双键
与H2加成后的产物是
 ,则该烯烃的结构式可能有( )
,则该烯烃的结构式可能有( )A. 1种 B. 2种 C. 3种 D. 4种
难度: 简单查看答案及解析
-
乙醇分子中各化学键如图所示.下列关于乙醇在不同的反应中断裂化学键的说法错误的是
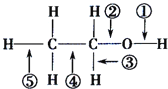
A. 与金属钠反应时,键①断裂
B. 在加热和Cu催化下与O2反应时,键①、③断裂
C. 与浓硫酸共热发生消去反应时,键②③断裂
D. 与乙酸、浓硫酸共热发生酯化反应时,键①断裂
难度: 简单查看答案及解析