-
下列不属于“低碳生活”方式的是( )
A. 尽量使用太阳能等代替化石燃料
B. 减少使用一次性筷子
C. 实行数字化办公减少纸张使用
D. 超市购物塑料袋有偿使用
难度: 简单查看答案及解析
-
下列有关实验室制取蒸馏水的实验装置与操作的说法中,错误的是( )
A. 冷凝管中水流方向是从下口进入,上口排出
B. 温度计的水银球应插入蒸馏烧瓶的自来水中
C. 实验中需要在烧瓶中加入几粒碎瓷片,防止出现暴沸现象
D. 蒸馏烧瓶必须垫加石棉网加热
难度: 简单查看答案及解析
-
下列分离方法错误的是( )
A. 除去混在植物油中的水——倾倒
B. 除去粗盐中的泥沙——过滤
C. 用乙醚提取中草药中的有效成分——萃取
D. 从海水中获得淡水——蒸馏
难度: 简单查看答案及解析
-
下列实验方案设计中,正确的是( )
A. 用酚酞指示剂区别氢氧化钠溶液和碳酸钠溶液
B. 用点燃的火柴在液化气钢瓶口检验是否漏气
C. 用澄清石灰水检验某溶液中是否含有CO32-
D. 用盐酸和BaCl2溶液检验某溶液中是否含有SO42-
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 同温同压下,任何气体的分子间平均距离几乎相等
B. 标准状况下,22.4L CCl4的物质的量是1mol
C. 等物质的量的O2和O3中所含有的氧原子数相同
D. 等物质的量浓度的MgCl2溶液和CaCl2溶液中所含有的离子数相同
难度: 简单查看答案及解析
-
下列有关物质的性质与用途具有对应关系的是( )
A. FeCl3易溶于水,可用作净水剂
B. 焦炭具有还原性,可用作脱色剂
C. H2O2易分解,实验室可用于制取少量氧气
D. NH4HCO3受热易分解,可用作氮肥
难度: 简单查看答案及解析
-
下列离子方程式中,正确的是( )
A. 氯气跟氯化亚铁溶液反应生成氯化铁:Fe2++Cl2=Fe3++2Cl-
B. 铜跟稀硝酸反应,产物之一是硝酸铜:Cu+2H+=Cu2++H2↑
C. 碳酸氢钠溶液跟醋酸反应:HCO3-+H+=CO2↑+H2O
D. 碳酸钙跟稀盐酸反应:CaCO3+2H+=Ca2++CO2↑+H2O
难度: 简单查看答案及解析
-
下列各组中的离子能在溶液中大量共存的是( )
A. Na+、Mg2+、Cl-、NO3- B. SO42-、Fe2+、K+、OH-
C. Ba2+、Cu2+、SO42-、Cl- D. HCO3-、CO32-、K+、H+
难度: 简单查看答案及解析
-
下列反应中,不属于氧化还原反应的是( )
A. 3NO2+H2O=2HNO3+NO B. FeCl3+3H2O(沸水)
Fe(OH)3(胶体)+3HCl
C. SiO2+3C
SiC+2CO↑ D. Cu2O+2HCl=Cu+CuCl2+H2O
难度: 简单查看答案及解析
-
下列图示装置和原理能达到实验目的的是( )
A. 实验室制取O2

B. 分离H2和CO2

C. 分离铁粉和铜粉
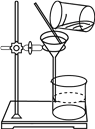
D. 浓缩FeCl3溶液
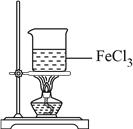
难度: 中等查看答案及解析
-
为除去粗盐中的Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作。其中正确的操作顺序是( )
①过滤;②加NaOH溶液;③加盐酸;④加Na2CO3溶液;⑤加BaCl2溶液。
A. ②③④⑤① B. ④①②⑤③ C. ②⑤④①③ D. ④③⑤②①
难度: 简单查看答案及解析
-
下列说法正确的是( )
A. 若H2O2分解产生1mol O2,理论上转移的电子数约为4NA
B. 1.8g的NH4+离子中含有的电子数为0.11 NA
C. 通常条件下,11.2L氧气中所含有的原子数为NA
D. 通常条件下,10.0mL水中所含分子数约为0.556NA
难度: 中等查看答案及解析
-
RO32-+2Rx+6H+=3R+3H2O是某同学写出的一个离子方程式,其中Rx所带电荷模糊不清,若R所带电荷用x表示,则x应是( )
A. +1 B. 2- C. 3+ D. 4-
难度: 中等查看答案及解析
-
ClO2是一种广谱型的消毒剂。工业上ClO2常用NaClO3和NaSO3溶液并加H2SO4酸化后反应制得,在以上反应中NaClO3和Na2SO3的个数之比为( )
A. 1:1 B. 2:1 C. 1:2 D. 2:3
难度: 简单查看答案及解析
-
引燃密闭容器中的己烷(C6H14)和氧气的混合气体,使其发生不完全燃烧反应。在500℃时测得反应前后气体的压强分别为270mm Hg和390mm Hg。试根据上述实验的数据判断这一燃烧反应主要是按下列哪个化学方程式进行的( )
A. C6H14+9O2=CO+5CO2+7H2O B. C6H14+7O2=5CO+CO2+7H2O
C. C6H14+8O2=3CO+3CO2+7H2O D. 2C6H14+15O2=8CO+4CO2+14H2O
难度: 中等查看答案及解析
-
为验证人体呼出气体中含有的CO2不是来自空气,而是人体代谢作用产生的。某学校学生课外活动小组设计了如图所示装置,你认为该装置应选用的试剂是( )

A. I是NaOH溶液 II.是Ca(OH)2溶液
B. I是Ca(OH)2溶液 II.是NaOH溶液
C. I是稀盐酸 II.是Ca(OH)2溶液
D. I是NaOH溶液 II.是CaCl2溶液
难度: 中等查看答案及解析
