-
在下列各溶液中,离子可能大量共存的是( )
A.无色溶液中:Al3+、Na+、SO42-、AlO2-
B.澄清透明的溶液中:Cu2+、Fe3+、NO3-、Cl-
C.含有大量ClO-的溶液中:K+、H+、I-、SO32-
D.水电离产生的c(H+)=10-12mol•L-1的溶液中:Na+、Fe2+、SO42-、NO3-难度: 中等查看答案及解析
-
下列说法正确的是( )
A.没有光纤就没有互联网,光纤的主要成分是硅
B.碳酸钠具有碱性,医疗上可用来治疗胃酸过多
C.煤气化技术的使用,不能减少二氧化碳的排放
D.大量使用家用汽车替代公交,能有效保护环境难度: 中等查看答案及解析
-
已知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ•mol-1;HCl(aq)与NaOH(aq)中和反应的△H=-55.6kJ•mol-1.则HCN在水溶液中电离的△H等于( )
A.+43.5kJ•mol-1
B.-43.5kJ•mol-1
C.-67.7kJ•mol-1
D.+67.7kJ•mol-1难度: 中等查看答案及解析
-
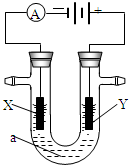
如图所示的实验原理、方法、装置或操作正确的是( )
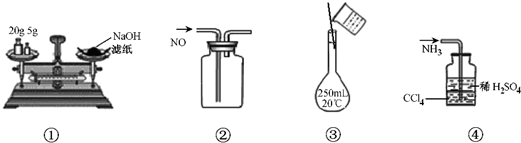
A.①称量氢氧化钠固体
B.②收集NO气体
C.③配制100mL0.10mol•L-1盐酸
D.④吸收NH3不会造成倒吸难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
A.常温常压下11gCO2中共用电子对的数目为NA
B.11.2L乙烯、乙炔的混合物中C原子数为NA
C.1L1mol•L-1Na2CO3溶液中含CO32-离子数为NA
D.1mol乙醇和1mol乙酸反应生成的水分子数为NA难度: 中等查看答案及解析
-
下列解释实验事实的方程式不正确的是( )
A.0.1mol/LCH3COOH溶液的pH>1:CH3COOH⇌CH3COO-+H+
B.“NO2球”浸泡在冷水中,颜色变浅:2NO2(g)(红棕色)⇌N2O4(g)(无色)△H<0
C.铁溶于稀硝酸,溶液变黄:3Fe+8H++2NO3-⇌3Fe2++2NO2+4H2O
D.向Na2CO3溶液中滴入酚酞,溶液变红:CO32-+H2O⇌HCO3-+OH-难度: 中等查看答案及解析
-
T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示.则下列结论正确的是( )
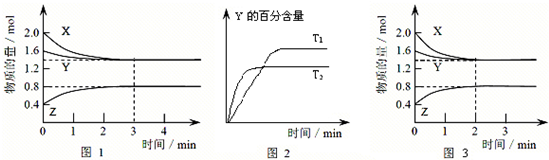
A.反应进行的前3min内,用X表示的反应速率v(X)=0.3mol•-1
B.容器中发生的反应可表示为:3X(g)+Y(g)2Z(g)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强难度: 中等查看答案及解析