-
一定温度下,浓度均为0.1mol/L的下列溶液中,含H+离子浓度最小的是( )
A.CH3COOH B.H2SO4 C.HNO3 D.HCl
难度: 简单查看答案及解析
-
下列试纸,使用时预先不能用蒸馏水润湿的是 ( )
A. 红色石蕊试纸 B. 蓝色石蕊试纸
C. 淀粉KI试纸 D. pH试纸
难度: 简单查看答案及解析
-
常温下,下列溶液的pH大于7的是 ( )
A.NH4Cl B.H3PO4 C.NaHCO3 D.Na2SO4
难度: 简单查看答案及解析
-
将纯水加热至较高温度,下列叙述正确的是 )
A.KW变大,pH变小,呈酸性
B.KW不变,pH不变,呈中性
C.KW不变,pH变大,呈碱性
D.KW变大,pH变小,呈中性
难度: 简单查看答案及解析
-
25 ℃时,0.05mol/L的Ba(OH)2溶液的pH为 ( )
A. 12.7 B. 12.0 C. 13.0 D.13.7
难度: 简单查看答案及解析
-
25℃时,某溶液中由水电离出的c(OH—)=1×10—13 mol/L,该溶液中一定不能大量共存的离子组是 ( )
A. NH4+
、HCO3— 、SO42— 、Cl—
B. CO32— 、Cl—
、K+ 、Na+
C. Na+ 、SO42— 、CO3— 、Cl—
D. SO42—、Fe3+ 、 Na+ 、K+
难度: 简单查看答案及解析
-
Mg(OH)2在水中存在溶解平衡Mg(OH)2(s)
Mg2+(aq)+20H﹣(aq),要使Mg(OH)2进一步溶解,应向溶液中加少量的固体是 ( )
A.NH4Cl B.NaOH C.MgCl2 D.Fe
难度: 简单查看答案及解析
-
下列关于电解池的叙述中,不正确的是 ( )
A.与电源正极相接的是电解池的阴极
B.与电源负极相接的是电解池的阴极
C.电解池的阳极发生氧化反应
D.电子从电
源的负极沿导线流向电解池的阴极
难度: 中等查看答案及解析
-
理论上不能用于设计成原电池的化学反应是 ( )
A. 4Fe(OH)2(s)+2H2O(l)+O2(g)===4Fe(OH)3(s)ΔH<0
B.CH3CH2OH(l)+3O2(g)===2CO2 (g)+3H2O(l) ΔH<0
C.Al(OH)3(s)+NaOH(aq)===NaAlO2(aq)+2H2O(l)ΔH<0
D.H2(g)+Cl2(g)===2HCl(g)ΔH<0
难度: 中等查看答案及解析
-
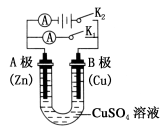
在盛有稀H2SO4的烧杯中放入用导线连接的锌片和铜片,下列叙述正确的是( )
A.SO42-离子移向正极
B.电子通过导线由铜片流向锌片
C.正极有O2逸出
D.铜片上有H2逸出
难度: 中等查看答案及解析
-
在原电池和电解池的电极上所发生的反应,同属还原反应的是 ( )
A.原电池正极和电解池阳极所发生的反应
B.原电池正极和电解池阴极所发生的反应
C.原电池负极和电解池阳极所发生的反应
D.原电池负极和电解池阴极所发生的反应
难度: 中等查看答案及解析
-
有A、B、C、D四种金属,当A、B组成原电池时,电子流动方向A →B ;当A、D组成原电池时,A为正极;B与E构成原电池时,电极反应式为:E2-+2e-=E,B-2e-
=B2+则A、B、D、E金属性由强到弱的顺序为( )
A.A﹥B﹥E﹥D B.D﹥A﹥B﹥E C.D﹥E﹥A﹥B D.A﹥B﹥D﹥E
难度: 中等查看答案及解析
-
在相同温度下用惰性电极电解下列溶液,一段时间后溶液酸性增强的是( )
A.HCl B.NaOH C.Na2SO4 D.CuSO4
难度: 中等查看答案及解析
-
在铁制品上镀上一定厚度的铜层,以下电镀方案中正确的是 ( )
A.铜作阳极,铁制品作阴极,溶液中含Fe2+
B.铜作阴极,铁制品作阳极,溶液中含Cu2+
C.铜作阴极,铁制品作阳极,溶液中含Fe3+
D.铜作阳极,铁制品作阴极,溶液中含Cu2+
难度: 中等查看答案及解析
-
下列叙述不正确的是 ( )
A.原电池
是将化学能转化为电能的装置
B.铁船底镶嵌锌块,锌作负极,以防船体被腐蚀
C.钢铁腐蚀的负极反应:Fe-3e-===Fe3+
D.把锌片放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快
难度: 中等查看答案及解析
-
某原电池装置如图所示。下列有关叙述中,正确的是 ( )
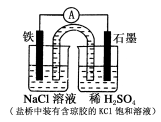
A.Fe作正极,发生氧化反应
B.负极反应:2H++2e-===H2↑
C.工作一段时间后,两烧杯中溶液pH均不变
D.工作一段时间后,NaCl溶液中c(Cl-)增大
难度: 中等查看答案及解析
-
下列表述正确的是( )
A.电解饱和食盐水时,阳极的电极反应式为:2Cl- - 2e- =Cl2 ↑
B.酸性介质和碱性介质的氢氧燃料电池的正极反应式均为:O2 + 2H2O + 4e- =4OH –
C.粗铜精炼时,与电源正极相连的是纯铜,电极反应式为:Cu-2e- =Cu2+
D.钢铁发生电化学腐蚀的正极反应式:Fe-2e- =Fe2+
难度: 中等查看答案及解析
-
如图是电解CuCl2溶液的装置,其中c、d为石墨电极。则下列有关的判断正确的是( )
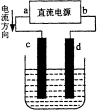
A.a为负极、b为正极
B. a为阳极、b为阴极
C. 电解过程中,氯离子浓度不变
D. 电解过程中,d电极质量增加
难度: 简单查看答案及解析
-
在25℃时;用石墨电极
电解 CuSO4溶液(假设溶液的体积在电解前后不发生变化)。5 min后,在一个石墨电极上有6.4 g Cu生成。下列说法中正确的是 ( )
A.有Cu生成的一极是阴极,发生氧化反应
B.反应中转移电子的物质的量为0.4 mol
C.在另一极得到O2的体积(标准状况)是1.12 L
D.电解一段时间后,溶液的pH不变
难度: 简单查看答案及解析
-
pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强碱与强酸的体积比( )
A.11
:1 B.9 :1 C.1 :11 D.1 :9
难度: 简单查看答案及解析