-
氧是地壳中含量最多的元素,已知一种氧原子,原子核外含有8个质子和10个中子,则该氧原子核外电子数为( )
A.2
B.8
C.10
D.18难度: 中等查看答案及解析
-
空气成分中,体积分数最大的是( )
A.氮气
B.二氧化碳
C.氧气
D.稀有气体难度: 中等查看答案及解析
-
C3N4是一种新型材料,它的硬度比金刚石还高,可做切割工具.在C3N4中,C的化合价为+4,则N的化合价是( )
A.+5
B.+3
C.+1
D.-3难度: 中等查看答案及解析
-
将密封良好的方便面从平原带到高原时,包装袋鼓起,是因为袋内的气体分子( )
A.间隔增大
B.质量增大
C.体积增大
D.个数增多难度: 中等查看答案及解析
-
地壳中含量最多的金属元素是( )
A.硅
B.氧
C.铝
D.铁难度: 中等查看答案及解析
-
下列物质中,含有氧分子的是( )
A.O2
B.H2O
C.CO2
D.SO2难度: 中等查看答案及解析
-
下列变化中,属于化学变化的是( )
A.矿石粉碎
B.纸张燃烧
C.酒精挥发
D.冰雪融化难度: 中等查看答案及解析
-
下列物质中,属于溶液的是( )
A.牛奶
B.豆浆
C.冰水
D.糖水难度: 中等查看答案及解析
-
下列物质在氧气中燃烧,火星四射,有黑色固体生成的是( )
A.红磷
B.木炭
C.甲烷
D.铁丝难度: 中等查看答案及解析
-
实验室熄灭酒精灯是用灯帽将其盖灭,该灭火方法的主要原理是( )
A.隔绝空气
B.降低温度
C.清除可燃物
D.降低可燃物的着火点难度: 中等查看答案及解析
-
下列物质中,属于纯净物的是( )
A.冰镇啤酒
B.新鲜空气
C.优质燃煤
D.干冰难度: 中等查看答案及解析
-
下列物质的主要成分属于氧化物的是( )
A.
钻石(C)
B.
水晶(SiO2)
C.
食盐(NaCl)
D.
钟乳石(CaCO3)难度: 中等查看答案及解析
-
成人体内99%的钙存在于骨骼和牙齿中,这里的“钙”是指( )
A.原子
B.分子
C.元素
D.单质难度: 中等查看答案及解析
-
天然气的主要成分是甲烷,甲烷由碳、氢两种元素组成,这两种元素的本质区别是( )
A.质子数不同
B.电子数不同
C.中子数不同
D.最外层电子数不同难度: 中等查看答案及解析
-
冬季室内燃煤取暖时,要注意保持通风,以免造成人员中毒.这里的有毒气体主要是指( )
A.O2
B.N2
C.CO
D.CO2难度: 中等查看答案及解析
-
下列物质由原子直接构成的是( )
A.铁
B.氧气
C.二氧化硫
D.食盐难度: 中等查看答案及解析
-
下列化学符号中,表示正确的是( )
A.2个镁原子:2Mg
B.钙离子:Ca+2
C.2个氧原子:O2
D.氯化铝:A1C1难度: 中等查看答案及解析
-
下列图标中,与消防安全无关的是( )
A.
B.
C.
D.
难度: 中等查看答案及解析
-
下列操作中,能鉴别空气、氧气和氢气3瓶气体的是( )
A.观察气体颜色
B.倒入澄清石灰水
C.闻气体的气味
D.插入燃着的木条难度: 中等查看答案及解析
-
如图是元素周期表中银元素的信息示意图,对图中信息理解不正确的是( )

A.该元素为金属元素
B.相对原子质量为107.9
C.元素符号为Ag
D.质子数和中子数均为47难度: 中等查看答案及解析
-
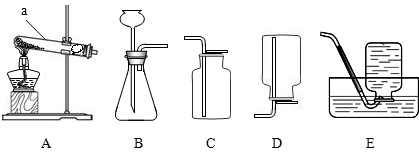
下列实验操作中,正确的是( )
A.
点燃酒精灯
B.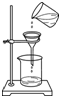
过滤
C.
加热液体
D.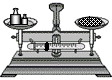
称量固体难度: 中等查看答案及解析
-
下列关于物质的性质和用途说法中,不正确的是( )
A.氧气具有可燃性,用于火箭发射
B.洗洁精具有乳化作用,用于去除油污
C.氮气常温下化学性质稳定,用于食品防腐
D.稀有气体在通电时会发出不同颜色的光,用于制成各种灯具难度: 中等查看答案及解析
-
如图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号.下列有关该实验的说法中,正确的是( )
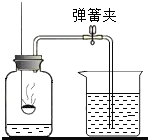
A.弹簧夹没夹紧不会对实验结果产生影响
B.燃烧匙内盛放过量的红磷会导致实验结果偏大
C.没等装置冷却就打开弹簧夹会导致实验结果偏大
D.点燃红磷伸入瓶中时,没有立即塞紧瓶塞会导致实验结果偏大难度: 中等查看答案及解析
-
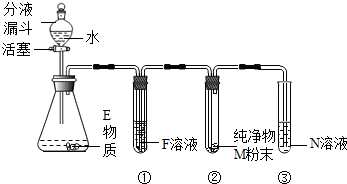
如图装置可用于气体的收集、检验和体积的测量等,不能完成的实验是( )
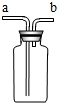
A.气体从a端通入,收集氧气
B.瓶内装满水,气体从b端通入,收集氧气
C.在b端接量筒,瓶内装满水,测量二氧化碳的体积
D.瓶内装有澄清石灰水,检验氧气中是否混有二氧化碳难度: 中等查看答案及解析
-
下列图象中,能正确反映对应变化关系的是( )
A.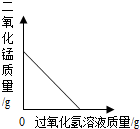
向一定量的二氧化锰中加入过氧化氢溶液
B.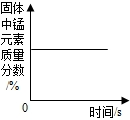
加热一定量的高锰酸钾固体
C.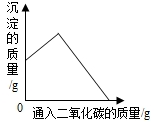
向一定量的澄清石灰水中通入二氧化碳
D.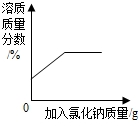
20℃时,向一定量接近饱和的氯化钠溶液中加入氯化钠固体难度: 中等查看答案及解析