-
如果你家里的食用豆油混有一些水,你将采用下列何种方法分离
A.过滤 B.分液 C.萃取 D.蒸馏
难度: 简单查看答案及解析
-
下列操作中不正确的是
A.过滤时玻璃棒与三层滤纸处接触
B.酒精和水的混合物可以通过蒸馏将二者分离开来
C.向试管中滴加液体时,胶头滴管应紧贴试管内壁
D.KNO3中混有少量的NaCl,可通过重结晶实验将杂质除去
难度: 中等查看答案及解析
-
下列叙述正确的是
A.1 mol H2O的质量为18g
B.摩尔是表示物质微粒数目的一个物理量
C.3.01×1023个SO2分子的质量为64g
D.标准状况下,1 mol任何物质体积均约为22.4L
难度: 中等查看答案及解析
-
在5L物质的量浓度为2mol/l的K2SO4溶液中K+的物质的量浓度为
A.2mol/l B.4mol/l C.1 mol/l D.20mol/l
难度: 简单查看答案及解析
-
有一种气体的质量是14.2g,体积是4.48升(标准状况),该气体的摩尔质量是
A.28.4 g B.28.4g·mol-1
C.71 g·mol-1 D.71 g
难度: 中等查看答案及解析
-
实验中的下列操作正确的是
A.用试管取出试剂瓶中的K2CO3溶液,发现取量过多,又把过量的试剂倒入试剂瓶中
B.Cu(NO3)2 溶于水,可将含有Cu(NO3)2 的废液倒入水槽中,再用水冲入下水道
C.用浓硫酸配制一定物质的量浓度的稀硫酸时,浓硫酸溶于水后,应冷却至室温才能转移到容量瓶中
D.用蒸发方法使NaCl 从溶液中析出时,应将蒸发皿中NaCl 溶液全部加热蒸干
难度: 中等查看答案及解析
-
用NA表示阿伏加德罗常数,下列叙述正确的是
A.常温常压下,1.06g Na2CO3含有的Na+离子数目为0.02 NA
B.常温常压下,2NA 个CO2分子占有的体积为44.8L
C.标准状况下,22.4LH2O含有的分子数为 NA
D.物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl- 个数为 NA
难度: 中等查看答案及解析
-
过滤后的食盐水仍含有可溶性的CaCl2、MgCl2、Na2SO4 等杂质,通过如下几个实验步骤,可制得纯净的食盐水:
①加入稍过量的Na2CO3溶液;
②加入稍过量的NaOH溶液;
③加入稍过量的BaCl2 溶液;
④滴入适量的稀盐酸至无气泡产生;
⑤过滤。正确的操作顺序是
A.③⑤②①④ B.①②③⑤④
C.②③①④⑤ D.③②①⑤④
难度: 中等查看答案及解析
-
科学家已发现一种新型氢分子,其化学式为H3,在相同条件下,等质量的H3和H2相同的是
A.体积 B.分子数
C.原子数 D.物质的量
难度: 中等查看答案及解析
-
同体积同物质的量浓度的几种可溶性盐的溶液中,一定具有相同的
A.溶质的摩尔质量 B.溶质的质量
C.溶质的物质的量 D.离子总数
难度: 中等查看答案及解析
-
欲配制100ml 1.0 mol/L Na2SO4溶液,正确的方法是
①将32.2g Na2SO4·10H2O溶于少量水中,再用水稀释至100 ml
②将14.2 g Na2SO4 溶于100ml水中制成溶液
③将20 ml 5.0 mol/L Na2SO4溶液用水稀释至100 ml
A.①② B.①②③
C.①③ D.②③
难度: 中等查看答案及解析
-
同温同压下两个容积相等的贮气瓶,一个装有CO,一个装有N2和C2H4的混合气体,两瓶气体一定不相同的是
A.分子总数 B.总质量 C.原子总数 D.密度
难度: 中等查看答案及解析
-
用10 mL的0.1 mol·L-1 BaCl2溶液恰好可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是
A.3∶2∶2 B.1∶3∶3 C.1∶2∶3 D.3∶1∶1
难度: 中等查看答案及解析
-
能够用来鉴别BaCl2、NaCl、Na2CO3三种物质的试剂是
A.稀硫酸 B.AgNO3溶液 C.稀盐酸 D.稀硝酸
难度: 中等查看答案及解析
-
在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的
A.
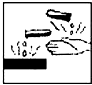 B.
B.
C.
 D.
D.难度: 简单查看答案及解析
-
下列溶液中,与100 ml 0.5 mol/L NaCl溶液所含的Cl-的物质的量浓度相同的是
A、100 ml 0.5 mol/L MgCl2 溶液
B、200 ml 0.25 mol/L CaCl2溶液
C、50 ml 1 mol/L NaCl溶液
D、200 ml 0.25 mol/L HCl溶液
难度: 中等查看答案及解析
-
下列有关说法错误的是
A.NA 个OH-含有电子10mol
B.某元素R一个原子的质量是ag,则其的相对原子质量可表示为a NA
C.4L0.5mol/L的NaOH溶液中含有阴离子的数目为2NA
D.配制一定物质的量浓度的NaOH溶液时,定容时俯视操作所得溶液浓度偏低
难度: 中等查看答案及解析
-
在两个密闭容器中,分别充有质量相同的甲、乙两种气体,若两容器的温度和压强均相同,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多
B.甲的摩尔体积比乙的摩尔体积小
C.甲的相对分子质量比乙的相对分子质量小
D.甲的物质的量比乙的物质的量少
难度: 中等查看答案及解析