-
将适量铁粉放入FeCl3溶液中,完全反应后,所得溶液中Fe3+和Fe2+物质的量浓度之比为1:3,则已反应的Fe3+与未反应的Fe3+的物质的量之比是( )
A. 1:1 B. 3:2 C. 2:1 D. 2:3
难度: 简单查看答案及解析
-
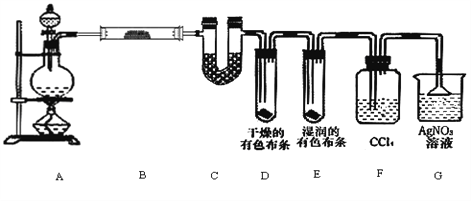
检验氯化氢气体中是否混有Cl2,可采用的方法是( )
A. 用干燥的蓝色石蕊试纸
B. 用干燥有色布条
C. 将气体通入硝酸银溶液
D. 用湿润的淀粉碘化钾试纸
难度: 中等查看答案及解析
-
下列关于钠及其化合物的说法不正确的是
A. 金属钠与O2反应,条件不同,产物不同
B. 钠、氧化钠、过氧化钠暴露在空气中最终都会转化为碳酸钠
C. 少量的钠可保存在有机溶剂CCl4中
D. 1molNa2O2与足量水反应,转移1mol电子
难度: 简单查看答案及解析
-
下列反应中,水只作还原剂的是
A. 2Na2O2+2H2O=4NaOH+O2↑ B. 2Na+2H2O=2NaOH+H2↑
C. 2F2 + 2H2O = 4HF + O2 D. 2H2O
2H2↑+O2↑
难度: 简单查看答案及解析
-
下列物质中,不能使有色布条褪色的是
A. Cl2 B. 氯水 C. NaClO溶液 D. Na2O2与水反应后的溶液
难度: 简单查看答案及解析
-
将铁放入下列溶液中,溶液的质量会减少的是
A. 盐酸溶液 B. 硫酸锌溶液 C. 硫酸铁溶液 D. 硫酸铜溶液
难度: 简单查看答案及解析
-
制取氯水最好的方法是
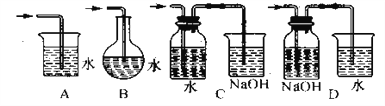
A. A B. B C. C D. D
难度: 简单查看答案及解析
-
分别往含有下列离子的溶液中通入氯气,离子浓度不会减少的是
A. H+ B. HCO3- C. Br- D. Ag+
难度: 简单查看答案及解析
-
下列物质中不能与氢氧化钠反应的是
A. Cl2 B. 碳酸氢钠 C. 氢氧化铝 D. 氧化铁
难度: 简单查看答案及解析
-
除去FeCl2溶液中FeCl3和CuCl2杂质可选用
A. NaOH B. Cl2水 C. Fe粉 D. Mg粉
难度: 简单查看答案及解析
-
下列关于等质量Na2CO3和NaHCO3的比较中正确的是( )
A. 热稳定性:Na2CO3<NaHCO3
B. 常温时水溶解性:Na2CO3<NaHCO3
C. 与足量盐酸反应产生CO2的量:Na2CO3<NaHCO3
D. 与足量盐酸反应消耗HCl的量:Na2CO3<NaHCO3
难度: 简单查看答案及解析
-
下列说法正确的是
A. 铝盐和铁盐都可以作净水剂.
B. 在饱和Na2CO3溶液中通入CO2没有任何现象
C. 将CO2通入CaCl2溶液中至饱和,有沉淀产生
D. 用澄清石灰水可区别Na2CO3和NaHCO3粉末
难度: 中等查看答案及解析
-
下列物质①NaHCO3 ②Al ③Fe2O3 ④Al(OH)3 ⑤MgO中,既能与盐酸反应,又能与氢氧化钠溶液反应的是( )
A. ②③④ B. ①④⑤ C. ①②④ D. 全部
难度: 简单查看答案及解析
-
甲、乙、丙三瓶溶液分别为NaCl、NaBr、KI,向甲中加入淀粉溶液和氯水,则溶液变为橙色,再加入丙溶液,颜色无明显变化,则甲、乙、丙依次含有
A. NaBr NaCl KI B. NaBr KI NaCl
C. KI NaBr NaCl D. NaCl KI NaBr
难度: 中等查看答案及解析
-
下列离子方程式正确的是
A. 硫酸铝溶液与过量氨水反应:Al3++3OH- =Al(OH)3↓
B. Na2CO3溶液中滴加少量盐酸:CO32-+2H+=H2O+CO2↑
C. FeCl2溶液跟Cl2反应:Fe2++Cl2 = Fe3+ + 2Cl-
D. NaHSO4溶液与过量Ba(OH)2溶液反应:H++SO42-+Ba2++OH- = BaSO4↓+H2O
难度: 简单查看答案及解析
-
已知常温下氯酸钾与浓盐酸反应放出氯气,现按下图进行实验。玻璃管内装有分别滴有不同溶液的白色棉球,反应一段时间后,对图中指定部位颜色描述正确的是
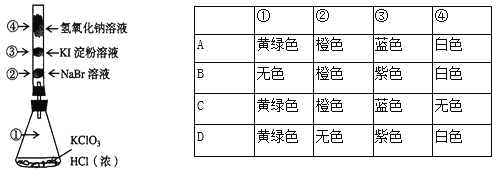
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
下列陈述Ⅰ、陈述Ⅱ均正确并且有因果关系的是
选项
陈述Ⅰ
陈述Ⅱ
A
NaHCO3溶于水能电离生成Na+和HCO3-
NaHCO3是电解质
B
Al2O3既可溶于盐酸,又能溶于烧碱溶液
Al2O3可用作耐火材料
C
铁比铝更易被腐蚀
铝比铁活泼
D
铝的最外层电子较钠多
钠的金属性强于铝
A. A B. B C. C D. D
难度: 中等查看答案及解析
-
把2.1 g CO与H2组成的混合气体与足量的O2充分燃烧后,立即通入足
量的Na2O2固体中,固体的质量增加( )
A. 2.1 g B. 3.6 g
C. 7.2 g D. 无法确定
难度: 中等查看答案及解析
-
将等物质的量的NaHCO3和Na2O2固体混合物置于密闭容器中,充分加热后,排出气体,最后剩余的固体为
A. Na2CO3 B. NaOH C. Na2CO3和NaOH D. Na2CO3和Na2O2
难度: 中等查看答案及解析
-
向Cu(NO3)2溶液中加入一定量的铁粉充分反应,下列情况中可能出现的是
①溶液中有Fe2+、Cu2+、不溶物为Cu ②溶液中有Fe2+、Cu2+、不溶物为Fe
③溶液中只有Cu2+、不溶物为Fe ④溶液中只有Fe2+、不溶物为Fe,Cu
A. ①③ B. ①④ C. ②③ D. ③④
难度: 中等查看答案及解析
-
由Na2O2、Na2CO3、NaHCO3、NaCl中某几种组成的混合物,向其中加入足量的盐酸有气体放出.将气体通过足量的NaOH溶液,气体体积减少一部分。将上述混合物在密闭容器中加热,有气体放出,下列判断正确的是
A. 混合物中一定不含有Na2CO3、NaCl B. 混合物中一定有Na2O2、NaHCO3
C. 无法确定混合物中是否含有NaHCO3 D. 混合物中一定不含Na2O2、NaCl
难度: 困难查看答案及解析