-
各种洗涤剂广泛进入人们的生活中,下列洗涤中所用洗涤剂具有乳化功能的是( )
A.用汽油除去衣服上的油污
B.用餐具洗洁精清洗餐具上的油污
C.用水洗去盘子中的水果渣
D.用醋洗去水壶的水垢难度: 中等查看答案及解析
-
地球是我们赖以生存的美丽家园,人类在生产和生活中的下列活动:①工业“三废”未经处理直接排放;②植树造林,加大绿化面积;③随意丢弃废旧电池和塑料制品垃圾;④生活污水任意排放;⑤减少空气中硫氧化物和氮氧化物的排放,防止形成酸雨.其中能对环境造成污染的是( )
A.③④⑤
B.②④⑤
C.①②⑤
D.①③④难度: 中等查看答案及解析
-
50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到218g固体(已换算成无水硫酸盐).则反应产生氢气的质量是( )
A.2g
B.3g
C.3.5g
D.4.5g难度: 中等查看答案及解析
-
2003年10月16日6时23分,“神舟”五号载人飞船在内蒙古成功着陆,返回舱完好无损.飞船在重返大气层时,由于同空气的剧烈摩擦,船体的表面温度将上升到2000℃~3000℃,因此飞船表面必须有良好的防高温措施.下列有关飞船的防高温措施中不可取的是( )
A.使用陶瓷类的贴面覆盖船体,以防止高温侵入舱内
B.使用在一定条件下能熔化或气化的表面覆盖材料
C.使用在-定条件下能与大气层中的氧气发生剧烈燃烧的表面覆盖材料
D.使用在一定条件下能发生分解反应的表面覆盖材料难度: 中等查看答案及解析
-
两位美国科学家彼得•阿格雷和罗德里克•麦金农,因为发现细胞膜水通道,以及对离子通道结构和机理研究作出的开创性贡献而获得2003年诺贝尔化学奖.他们之所以获得诺贝尔化学奖而不是生理学或医学奖是因为( )
A.他们的研究和化学物质水有关
B.他们的研究有利于研制针对一些神经系统疾病和心血管疾病的药物
C.他们的研究深入到分子、原子的层次
D.他们的研究深入到细胞的层次难度: 中等查看答案及解析
-
若在宇宙飞船的太空实验室(失重条件下)进行以下实验,其中最难完成的是( )
A.将金粉和铜粉混合
B.将牛奶加入水中混合
C.将氯化钠晶体溶于水中
D.用漏斗、滤纸过滤除去水中的泥沙难度: 中等查看答案及解析
-
在我们的日常生活中出现了“加碘食盐”、“增铁酱油”、“高钙牛奶”、“富硒茶叶”、“含氟牙膏”等商品,这里的碘、铁、钙、硒、氟应理解为( )
A.元素
B.原子
C.分子
D.单质难度: 中等查看答案及解析
-
可以一次性鉴别出蒸馏水、稀盐酸、石灰水的试剂是( )
A.酚酞试液
B.碳酸钠溶液
C.稀硫酸
D.氯化钠溶液难度: 中等查看答案及解析
-
家庭中常备的抗生素类药品“利君沙片”的相对分子质量为862,其中氢的质量分数为8.7%,则平均每个分子中含氢原子的数目为( )
A.87
B.86
C.75
D.23难度: 中等查看答案及解析
-
正常人胃液的pH在0.3~1.2之间,酸(一般以盐酸表示)多了,需要治疗.某些用以治疗胃酸过多的药物中含MgCO3、NaHCO3,还有用酒石酸钠来治疗的.这主要是由于( )
A.碳酸、酒石酸都不是强酸
B.对人体而言酒石酸是营养品
C.Na+、Mg2+都是人体必需的元素
D.MgCO3、NaHCO3与胃酸作用生成CO2,在服药后有喝汽水的舒服感难度: 中等查看答案及解析
-
下列变化中没有发生化学变化的是( )
A.剩饭变馊
B.自行车生锈
C.牛奶变酸
D.电灯发光难度: 中等查看答案及解析
-
光导纤维是将二氧化硅在高温下熔化、拉制成粗细均匀的光纤细丝,是信息高速公路的基础材料,在通讯、医疗、科技等领域都有广泛应用.二氧化硅(SiO2)属于( )
A.氧化物
B.酸
C.碱
D.盐难度: 中等查看答案及解析
-
纳米材料被誉为21世纪最有前途的新材料.纳米碳管是一种由碳原子构成的直径为几纳米(1nm=10-9m)的空心管.下列说法错误的是( )
A.纳米碳管在常温下化学性质稳定
B.纳米碳管是一种新型的化合物
C.纳米碳管材料管道多,表面积大,吸附能力强
D.纳米碳管材料如果完全燃烧,生成物是二氧化碳难度: 中等查看答案及解析
-
为了使经济可持续发展,生产过程应尽量减少对环境的负面作用.由单质铜制取硫酸铜有下列几种步骤,其中可行且符合以上要求的是( )
A.Cu→CuSO4
B.Cu→CuO→CuSO4
C.Cu→Cu2(OH)2CO3→CuSO4
D.Cu→Cu(NO3)2→Cu(OH)2→CuSO4难度: 中等查看答案及解析
-
温室中的绿色植物受阳光的照射生长,昼夜测定温室内氧气的含量如下图所示,其中正确的是( )
A.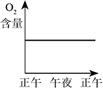
B.
C.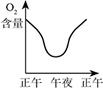
D.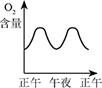
难度: 中等查看答案及解析