-
中国短道速滑队在索契冬奥会取得了骄人的成绩.速滑冰刀可用特种不锈钢制成,不锈钢含有的主要元素是

A.铁 B.碳 C.铜 D.铝
难度: 简单查看答案及解析
-
下列关于分散系的说法不正确的是
A.溶液、胶体、浊液属于不同的分散系
B.胶体与其他分散系的本质区别是胶体分散质粒子直径在1nm﹣100nm之间
C.可利用丁达尔现象鉴别溶液和胶体
D.利用过滤的方法可以分离胶体和溶液
难度: 中等查看答案及解析
-
硅的氧化物及硅酸盐构成了地壳中大部分的岩石、沙子和土壤.在无机非金属材料中,硅一直扮演着主角.下面几种物质中含有硅单质的是
A.
 玛瑙 B.
玛瑙 B. 光导纤维
光导纤维 C.
 太阳能电池板 D.
太阳能电池板 D. 水晶
水晶难度: 简单查看答案及解析
-
下图表示的是碳及其化合物之间的转化关系,下列说法正确的是
C
CO2
H2CO3
CaCO3
CO2.
A.反应①②③④均属于氧化还原反应
B.反应①中的单质C为还原剂
C.反应④中CaCO3既是氧化剂又是还原剂
D.反应①②③④所属的基本反应类型依次为:置换、复分解、化合、分解
难度: 中等查看答案及解析
-
只用一种试剂,可区别Na2SO4、AlCl3、NH4Cl、MgSO4四种溶液,这种试剂是
A.HCl B.BaCl2 C.AgNO3 D.NaOH
难度: 中等查看答案及解析
-
绿色植物是空气天然的“净化器”,研究发现,1公顷柳杉每月可以吸收160kg SO2,则1公顷柳杉每月吸收的SO2的物质的量为
A.164kg B.2.5mol C.2500mol D.2500g/mol
难度: 中等查看答案及解析
-
化学在生产和日常生活中有着重要的应用.下列说法不正确的是
A.根据冷的浓硫酸可以用铝质容器储存的事实,说明常温下铝不与浓硫酸发生反应
B.过氧化钠可作为防毒面具和潜水艇内的供氧计
C.可用稀硝酸鉴别铜锌合金制成的假金币
D.氢氟酸可用于雕刻玻璃
难度: 中等查看答案及解析
-
只由两种元素组成的化合物,其中一种元素是氢元素,这类化合物称氢化物.下列物质不属于氢化物的是
A.H2O B.H2SO4 C.NaH D.NH3
难度: 简单查看答案及解析
-
实验室需要用480mL 0.1mol•L﹣1的硫酸铜溶液,以下配制方法正确的是
A.称取12.5g胆矾(CuSO4•5H2O),配成500mL溶液
B.称取12.5g胆矾(CuSO4•5H2O),加入500mL水配成溶液
C.称取7.68g无水硫酸铜粉末,加入480mL水配成溶液
D.称取8.0g无水硫酸铜粉末,加入500mL水配成溶液
难度: 困难查看答案及解析
-
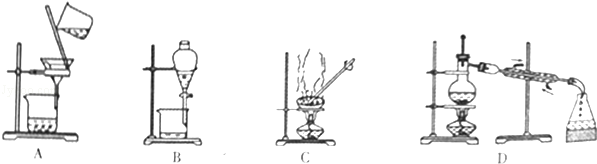
对I~IV的实验操作现象判断正确的是
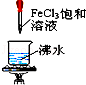
A.产生红褐色沉淀
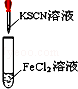
B.溶液颜色变红
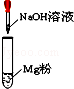
C.放出大量气体
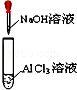
D.先出现白色沉淀,后沉淀又溶解
难度: 中等查看答案及解析
-
下列关于氧化还原反应的说法不正确的是
A.氧化还远反应的实质是电子的转移
B.含最高价元素的化合物均具有强氧化性
C.一定存在元素化合价的变化
D.氧化剂和还原剂混合不一定发生氧化还原反应
难度: 中等查看答案及解析
-
银耳本身为淡黄色,某地生产的一种“雪耳”,颜色洁白如雪.制作如下:将银耳堆放在密闭状态良好的塑料棚内,棚的一端支口小锅,锅内放有硫磺,加热使硫磺熔化并燃烧,两天左右,“雪耳”就制成了.“雪耳”炖而不烂,对人体有害,制作“雪耳”利用的是
A.硫的还原性
B.硫的漂白性
C.二氧化硫的还原性
D.二氧化硫的漂白性
难度: 简单查看答案及解析
-
N2O是一种有甜味、能溶于水、能助燃的无色气体,能刺激神经使人发笑,俗称“笑气”.现有等物质的量的“笑气”和二氧化碳,下列数值不一定相同的是
A.体积 B.质量 C.原子数 D.分子数
难度: 中等查看答案及解析
-
用NA表示阿伏伽德罗常数的值.下列叙述正确的是
A.标准状况下,22.4LO2中一定含有NA个氧原子
B.将80gNaOH溶于1L水中,所得溶液中NaOH的物质的量浓度为2mol/L
C.标准状况下,NA个H2O分子的体积是22.4L
D.3.4gNH3含有的分子数为0.2NA
难度: 困难查看答案及解析
-
X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收.已知X是化石燃料燃烧的产物之一,是形成酸雨的主要物质;Y是一种黄绿色气体单质,其水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应.下列说法不正确的是
A.X是SO2,它既有氧化性又有还原性
B.干燥的气体Y不能使干燥的有色布条褪色,其水溶液具有漂泊作用的是HClO
C.Z与水反应的化学方程式为:3NO2+H2O=2HNO3+NO
D.等物质的量的X与Y同时通入到湿润的有色布条上,有色布条褪色时间变短,漂泊效果增强
难度: 困难查看答案及解析
-
下列各组中的离子,能再溶液中大量共存的是
A.H+、Na+、HCO3﹣、Cl﹣
B.K+、Fe2+、Cl﹣、OH﹣
C.Ag+、Al3+、NO3﹣、H+
D.Fe3+、Al3+、SCN﹣、Cl﹣
难度: 中等查看答案及解析
-
下列离子方程式书写正确的是
A.钠和水反应:Na+H2O═Na++OH﹣+H2↑
B.铝与稀盐酸反应:2Al+6H+═2Al3++3H2↑
C.铜与氯化铁溶液反应:Fe3++Cu═Fe2++Cu2+
D.碳酸钙与稀盐酸反应:CO32﹣+2H+═CO2↑+H2O
难度: 中等查看答案及解析
-
向体积和物质的量浓度都相等的盐酸和氢氧化钠溶液中投入足量的铝粉,放出的氢气在同温同压下的体积之比为
A.1:1 B.1:3 C.2:3 D.1:2
难度: 中等查看答案及解析
-
我国“神舟七号”载人飞船的火箭燃料主要是偏二甲肼(用R表示)和四氧化二氮,在火箭发射时,两者剧烈反应产生大量气体并释放出大量的热,该反应的化学方程式为:R+2N2O4═3N2+4H2O+2CO2,下列叙述错误的是
A.此反应是氧化还原反应
B.R的分子式为C2H8N2
C.在反应中N2O4做还原剂
D.生成3mol N2时电子转移数为16mol
难度: 中等查看答案及解析
-
一定量的Cu和1mol•L﹣1 的稀硝酸反应,如果NO3﹣的浓度下降0.2mol•L﹣1,则溶液中c(H+)同时下降(假定反应前后溶液体积不变)
A.0.8mol•L﹣1 B.0.6mol•L﹣1 C.0.4mol•L﹣1 D.0.2mol•L﹣1
难度: 困难查看答案及解析